��Ŀ����
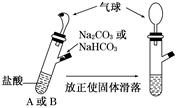
ij������������Al��(NH4)2SO4��MgCl2��FeCl2��AlCl3�е����ֻ�����ɣ��ֶԸû����������ʵ�飬����������й�������ͼ��ʾ(������������ѻ���ɱ�״���µ����)������˵���в���ȷ����( )
| A���ù�����һ��û��FeCl2�����ܺ���AlCl3 |
| B���ù����к���2��70 g Al |
| C���ù����к���6��60 g (NH4)2SO4 |
| D���ù����к���4��75 g MgCl2 |
A
�����������������Ϲ����м������Ũ��NaOH��Һ���ܹ������������Al��(NH4)2SO4 ������ֱ���H2��NH3��������ͨ����ʯ�Ҹ������������䣬��ͨ��Ũ���ᣬ���������С�Ҳ�Ϊ�㣬���Կ�֪���ɵ�����ΪH2��NH3 ������ֱ�Ϊ3��36L��2��3L��ԭ����������һ����Al��(NH4)2SO4 ����������Էֱ�����m(Al)=2��70g��m[(NH4)2SO4]=6��60g���ּ�����а�ɫ�������ɣ��Ұ�ɫ�������ò���ɫ����һ��û��FeCl2������ΪMg(OH)2��2��9g���ɴ˿ɼ����m(MgCl2)=4��75g���ɴ�m(Al)+m[(NH4)2SO4] +m(MgCl2)= 2��70g +6��60g +4��75g=14��05g�����Թ���������ֻ�����������ʣ�һ��û��AlCl3 ������A����ѡA��
���㣺���⿼��Ԫ�ػ��������ʺͼ��㡣

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д��ס������ձ��и�ʢ��100mL3mol/L�����������������Һ�������ձ��зֱ����A�˵����ۣ���Ӧ�����������ɵ��������Ϊ��:�ң�3:4������˵����ȷ����
| A���μӷ�Ӧ��H2SO4Ϊ0.2mol | B���μӷ�Ӧ��NaOHԼΪ0.27mol |
| C���������۵�����A��5.4 | D�������ᷴӦ�����۵�����7.2g |
��DZˮͧ������������Դ���ǣ� ��
| A����ѹ����ƿ | B��NaOH | C��Na2O2 | D��Na2CO3 |
ȡ16.8g̼�����ƹ��壬����һ��ʱ���ʣ����������Ϊ13.7g����ʣ�������뵽100mL 2mol/L��ϡ�����У���ַ�Ӧ����Һ��H+��Ũ��ԼΪ
| A��3 mol/L | B��2 mol/L | C��1.4 mol/L | D��1 mol/L |
��ͼ��ʾ����ԲȦ�ཻ�IJ��ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ�������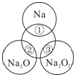
| A��Na2O2������������Ŀ֮��Ϊ1��1 |
| B����Ӧ�ٵ����ӷ���ʽΪ��Na+2H2O=Na++2OH��+H2�� |
| C����Ӧ������ܲ���0.05mol O2 |
| D���١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣��ڣ��� |
��һ���¶��£����ռ���Һ�з���һ�����Ĺ������ƣ���ַ�Ӧ��ָ���ԭ
�����¶ȣ�����˵����ȷ���ǣ� ��
| A����Һ��Na+Ũ��������O2�ų� | B����ҺPH���䣬��O2�ų��� |
| C����Һ��Na+��Ŀ���٣���O2�ų� | D����ҺPH������O2�ų� |
���й���̼���ƺ�̼�����Ƶ�������ȷ����
| A����ͬ�����£���ˮ�е��ܽ��ԣ�̼���� < ̼������ |
| B����ͬ�����£����ȶ��ԣ�̼���� > ̼������ |
| C����ͬ�����£����ᷴӦ�����ʣ�̼���� > ̼������ |
| D��һ�������£�̼���Ʋ���ת��Ϊ̼�����ƣ���̼�����ƿ���ת��Ϊ̼���� |
ijͬѧͨ��ϵ��ʵ��̽��Mg���仯��������ʣ� ������ȷ���ܴﵽĿ�ĵ���
������ȷ���ܴﵽĿ�ĵ���
| A����NaOH��Һ��������MgSO4��Һ�У��۲�Mg(OH)2���������� |
| B����ˮ����Ũ�����еõ�ϡ���ᣬ��þƬ������̽����Mg�Ļ����� |
| C����Mg(OH)2��Һֱ�ӵ�����װ����ֽ��©���й��ˣ�ϴ�Ӳ��ռ����� |
| D����Mg(OH)2����ת��������У�������ϡ���ᣬ�������ɵ���ˮMgCl2���� |