题目内容
取16.8g碳酸氢钠固体,加热一段时间后,剩余固体的质量为13.7g。把剩余固体加入到100mL 2mol/L的稀硫酸中,充分反应后溶液中H+的浓度约为
| A.3 mol/L | B.2 mol/L | C.1.4 mol/L | D.1 mol/L |
B
解析试题分析:根据反应结果分析,无论碳酸氢钠还是分解后的碳酸钠,钠原子量不变,根据产物硫酸钠得出反应的硫酸的量为钠原子量的一半(Na2SO4),故剩余硫酸的量为:0.1×2-16.8÷84÷2=0.1mol,反应后H+的浓度约为0.1mol×2÷0.1L="2" mol/L。
考点:考查溶液中离子浓度的计算有关问题。

练习册系列答案
相关题目
下列说法错误的是
| A.仅用KSCN可以检验Fe2+ | B.可以用NaOH溶液检验Fe3+ |
| C.通过化合反应可以得到Fe(OH)3 | D.通过化合反应可以得到FeCl2 |
为了验证Fe3+的性质,某化学兴趣小组设计了下图所示的一组实验,其中实验方案设计错误的是: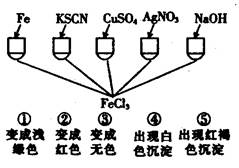
| A.只有④ |
| B.只有③ |
| C.③和④均错 |
| D.全部错误 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(v)与时间(t)关系如右图。反应中镁和铝的
| A.物质的量之比为3:2 | B.质量之比为3:2 |
| C.摩尔质量之比为2:3 | D.反应速率之比为2:3 |
下列有关金属及其化合物的说法正确的是
| A.NaHCO3的热稳定性大于Na2CO3 |
| B.FeCl3溶液能与铜反应,故可用于蚀刻印刷线路版 |
| C.Mg和Fe在一定条件下与水反应都生成氢气和对应的碱 |
| D.由于铝在空气中不会锈蚀,故铝制品的使用寿命都很长 |
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A.合金的熔点一般比组分金属低 |
| B.铝钠合金若投入一定量的水中可得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |
某固体混合物是由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):下列说法中不正确的是( )
| A.该固体中一定没有FeCl2,可能含有AlCl3 |
| B.该固体中含有2.70 g Al |
| C.该固体中含有6.60 g (NH4)2SO4 |
| D.该固体中含有4.75 g MgCl2 |
9.2 g金属钠投入到足量的重水中,则产生的气体中含有( )
| A.0.2 mol中子 | B.0.4 mol电子 | C.0.2 mol质子 | D.0.4 mol分子 |
小明在奥运五连环中填入了5种物质(如图所示),相连环的物质间所发生的反应中,没有涉及的基本反应类型是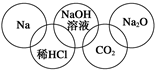
| A.分解反应 | B.复分解反应 |
| C.化合反应 | D.置换反应 |