题目内容
有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,A、B中分别有10 mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
A.A装置的气球膨胀速率大
B.若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L
C.若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L
D.最终两试管中Na+、Cl-的物质的量一定相同
C
解析试题分析:1.06g Na2CO3和0.84g NaHCO3的物质的量都是0.01nol。A、碳酸钠和酸反应分步进行,先生成碳酸氢钠,后碳酸氢钠和酸反应生成二氧化碳,所以A装置的气球膨胀速率小,错误; B、碳酸钠和酸反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2 ↑+H2O,碳酸氢钠和酸反应的离子方程式为HCO3-+H+=CO2 ↑+H2O;若最终两气球体积不同,所需酸的物质的量范围是:0<酸的物质的量<0.02mol,所以其浓度大于0小于2mol/L,错误; C、1.06g Na2CO3和0.84g NaHCO3的物质的量相同,若最终两气球体积相同,说明酸的物质的量大于或等于0.02mol,所以其浓度大于或等于2mol/L,正确; D、1.06g Na2CO3和0.84g NaHCO3的物质的量相同,所以Na2CO3和 NaHCO3中钠离子的物质的量不同,故最终两试管中Na+的物质的量一定不相同,故D错误。
考点:本题考查碳酸钠和碳酸氢钠的性质及计算。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案NaHCO3和Na2O2按1∶1的个数之比混合,在密闭容器中加热使之充分反应,然后趁热排出气体物质,容器内残留物的成分是
| A.Na2O2和NaHCO3 | B.NaHCO3和Na2CO3 |
| C.NaOH和Na2CO3 | D.只有Na2CO3 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(v)与时间(t)关系如右图。反应中镁和铝的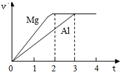
| A.物质的量之比为3:2 | B.质量之比为3:2 |
| C.摩尔质量之比为2:3 | D.反应速率之比为2:3 |
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A.合金的熔点一般比组分金属低 |
| B.铝钠合金若投入一定量的水中可得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |
某固体混合物是由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):下列说法中不正确的是( )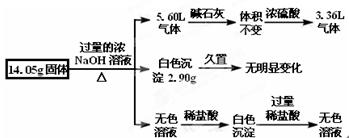
| A.该固体中一定没有FeCl2,可能含有AlCl3 |
| B.该固体中含有2.70 g Al |
| C.该固体中含有6.60 g (NH4)2SO4 |
| D.该固体中含有4.75 g MgCl2 |
向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,下列说法中正确的是( )
| A.溶液中的Na+总数不变 | B.溶液中的OH-数目不变 |
| C.溶质的物质的量浓度不变 | D.溶液的质量不变 |
9.2 g金属钠投入到足量的重水中,则产生的气体中含有( )
| A.0.2 mol中子 | B.0.4 mol电子 | C.0.2 mol质子 | D.0.4 mol分子 |
下列关于铝及其化合物的说法不正确的是
| A.Al既可用于食品包装,也可用做建筑材料 |
| B.Al2O3既可用来冶炼金属Al,也可用做耐火材料 |
| C.明矾[KAl(SO4)2·12H2O]既可用做净水剂,也可用作消毒剂 |
| D.Al(OH)3既可用作治疗胃酸过多的药物,也可用来制备一些铝盐 |
已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+H2O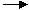 Y+H2
Y+H2 ↑;Z+H2O
↑;Z+H2O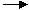 W+O2↑(方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
W+O2↑(方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
| A.X>Y Z>W | B.X<Y Z<W |
| C.X>Y Z<W | D.X<Y Z>W |