题目内容
5.下列物质的分类合理的是( )| A. | 氧化物:CO2、NO、SO2、 | B. | 碱:NaOH、KOH、Na2CO3 | ||
| C. | 铵盐:NH4Cl、NH4NO3、NH3•H2O | D. | 碱性氧化物:Na2O、CaO、Al2O3 |
分析 A、两种元素组成其中一种为氧元素的化合物为氧化物;
B、水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱;
C、含铵根离子的盐为铵盐;
D、和酸反应生成盐和水的氧化物为碱性氧化物,反应为复分解反应.
解答 解:A、CO2、NO、SO2符合氧化物概念,故A正确;
B、Na2CO3 属于盐,溶液显碱性是因为碳酸根离子水解,碳酸钠不是碱,故B错误;
C、NH4Cl、NH4NO3属于铵盐,NH3•H2O属于弱碱不是盐,故C错误;
D、Na2O、CaO属于碱性氧化物,Al2O3 属于两性氧化物和酸、碱都反应生成盐和水,故D错误;
故选A.
点评 本题考查了物质分类的方法和概念实质理解应用,注意物质组成和概念的判断依据,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
7.已知R-X+2Na+R′-X→R-R′+2NaX,若用CH3CH2Br和 (CH3)2CHBr 的混合物与金属钠反应,生成的烷烃不可能是( )
| A. | CH3CH2CH2CH3 | B. | CH3CH2CH2CH2CH3 | C. | (CH3)2CHCH(CH3)2 | D. | CH3CH2CH(CH3)2 |
16.下列表示的是有机化合物结构式中的一部分,其中不是官能团的是( )
| A. | -OH | B. | -C≡C- | C. |  | D. | C-C |
20.短周期元素A、B、C、D、E是同周期的五种元素,A和B的最高价氧化物对应水化物呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D,五种元素形成的简单离子中E的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A. | C、D、E、A、B | B. | E、C、D、A、B | C. | B、A、D、C、E | D. | B、A、E、D、C |
17.法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”.下列有关“四中子”粒子的说法不正确的是( )
| A. | 该粒子不显电性 | B. | 该粒子质量数为4 | ||
| C. | 与氢元素的质子数相同 | D. | 该粒子质量比氢原子大 |
14.如图图元素周期表的一部分,下列说法中正确的是( )
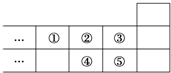

| A. | 元素①位于第2周期第ⅣA族 | |
| B. | ①的气态氢化物与⑤的气态氢化物反应产生白烟 | |
| C. | 元素的氧化物对应水化物的酸性一定是:⑤>④ | |
| D. | 元素的最高正化合价:③=⑤ |
 .
. ,EB4
,EB4 .
. ,
, .两种离子中,半径较小的是Na+(填离子符号).
.两种离子中,半径较小的是Na+(填离子符号). B2C2
B2C2 .
.