题目内容
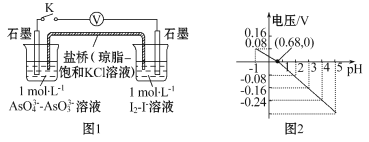
【题目】某实验小组依据反应AsO43-+2I-+2H+![]() AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
A.调节pH可以改变反应的方向
B.pH=0.68时,反应处于平衡状态
C.pH=5时, 负极电极反应式为2I--2e -= I2
D.pH>0.68时,氧化性I2>AsO43-
【答案】C
【解析】
试题分析:A、发生的反应AsO43-+2I-+2H+![]() AsO33-+I2+H2O为可逆反应,故调节pH(改变H+浓度)可以改变反应的方向,A正确;B、根据图示:当pH=0.68时,电压负为0,故反应处于相对静止状态,即化学平衡状态,B正确;C、pH=5时与pH=0.68时相比,H+浓度减小,平衡向逆反应方向移动,即发生AsO33-+I2+2OH-
AsO33-+I2+H2O为可逆反应,故调节pH(改变H+浓度)可以改变反应的方向,A正确;B、根据图示:当pH=0.68时,电压负为0,故反应处于相对静止状态,即化学平衡状态,B正确;C、pH=5时与pH=0.68时相比,H+浓度减小,平衡向逆反应方向移动,即发生AsO33-+I2+2OH-![]() AsO43-+2I-+H2O,该反应AsO33-发生氧化反应,为负极,故负极反应式AsO33-+H2O-2e-=AsO43-+2H+,C错误;D、pH>0.68时与pH=0.68时相比,H+浓度减小,平衡向逆反应方向移动,即发生AsO33-+I2+2OH-
AsO43-+2I-+H2O,该反应AsO33-发生氧化反应,为负极,故负极反应式AsO33-+H2O-2e-=AsO43-+2H+,C错误;D、pH>0.68时与pH=0.68时相比,H+浓度减小,平衡向逆反应方向移动,即发生AsO33-+I2+2OH-![]() AsO43-+2I-+H2O,该反应中I2为氧化剂,AsO43-为氧化产物,所以氧化性I2>AsO43-,D正确。答案选C。
AsO43-+2I-+H2O,该反应中I2为氧化剂,AsO43-为氧化产物,所以氧化性I2>AsO43-,D正确。答案选C。

练习册系列答案
相关题目







