题目内容
实验室中以下物质的贮存方法不正确的是( )
| A.少量液溴可用水封存,防止溴挥发 |
| B.少量金属钠保存在煤油中 |
| C.浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
| D.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 |
C
解析试题分析:浓硝酸能腐蚀橡胶塞,所以不能用橡胶塞,C项错误;液溴易挥发,用水封存可防止溴的挥发,故A项正确;钠在煤油中可防止空气中的氧气和水分与钠反应,B项正确;硫酸可防止硫酸亚铁水解,铁粉可防止硫酸亚铁被氧化,D项正确。
考点:本题考察试剂的保存。

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
下列有关试剂的保存方法,错误的是:
| A.金属钠保存在煤油中 |
| B.存放FeSO4溶液时加入少量铁粉 |
| C.NaOH溶液保存在带橡胶塞的玻璃试剂瓶中 |
| D.新制的氯水保存在无色细口瓶中 |
对含微量I-的某样品进行I-化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用Na2S2O3标准溶液滴定以求得I-的浓度。下列分析正确的是
已知:5I-+IO3-+6H+=3H2O+3I2 I-+3Br2(过量)+3H2O=6H++6Br-+IO3-
方法一I-(样品) IO3-
IO3-
 I2
I2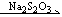 I-
I-
方法二I-(样品) I2
I2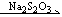 I-
I-
| A.方法二对样品所做处理操作简便,用作微量的测定更准确 |
| B.当待测液由无色变为蓝色时即达到滴定终点 |
| C.方法一与方法二测量出的样品浓度比为6:l |
| D.假设各步骤操作均得当,方法一所消耗Na2S2O3标准溶液的体积是方法二的6倍 |
下列实验方案可行或结论正确的是
| A.用饱和Na2CO3溶液除去CO2中的HCl |
| B.可用加热氯化铵的方法制取氨气 |
| C.用加热的方法可除去碳酸钠粉末中的碳酸氢钠 |
| D.在酸碱中和滴定实验中,当锥形瓶中溶液的颜色发生突变时即达到滴定终点 |
下列图示实验合理的是( ) 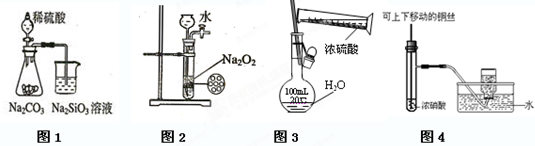
A.图1为证明非金属性强弱: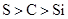 |
| B.图2为制备少量氧气 |
| C.图3为配制一定物质的量浓度的硫酸溶液 |
| D.图4为制备并收集少量NO2气体 |
下列说法正确的是
| A.在“食醋总酸含量的测定”实验中,选择酚酞溶液为指示剂,当溶液的颜色变为粉红色且在半分钟内不褪色,即达到滴定终点 |
| B.在“牙膏中某些主要成分的检验”实验中,在牙膏与蒸馏水搅拌、静置分离后的澄清溶液中加入少量的新制Cu(OH)2,当产生绛蓝色沉淀时,说明牙膏中含有甘油 |
| C.在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用酒精洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率。 |
| D.人体吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒;氨气、溴中毒休克时要马上进行人工呼吸 |
测定Cu(NO3)2·nH2O的结晶水含量,下列方案中不可行的是
| A.称量样品→加热→冷却→称量CuO |
| B.称量样品→加热→冷却→称量Cu(NO3)2 |
| C.称量样品→加NaOH→过滤→加热→冷却→称量CuO |
| D.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 |
下列根据实验操作及现象所得出的结论中,正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向两份蛋白质溶液中分别滴加NaCl溶液和 CuSO4溶液。均有固体析出 | 蛋白质均发生了变性 |
| B | 取少量Fe(NO3)2试样加水溶解,加稀硫酸酸化, 滴‘加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经 变质 |
| C | 将少量某物质的溶液滴加到新制的银氨溶液中, 水浴加热后有银镜生成 | 该物质一定属于醛类 |
| D | 同条件下,分别将0.1mol·L-1的盐酸和醋酸进 行导电性实验,与醋酸串联的灯泡较暗 | 醋酸是弱酸 |
