题目内容
对含微量I-的某样品进行I-化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用Na2S2O3标准溶液滴定以求得I-的浓度。下列分析正确的是
已知:5I-+IO3-+6H+=3H2O+3I2 I-+3Br2(过量)+3H2O=6H++6Br-+IO3-
方法一I-(样品) IO3-
IO3-
 I2
I2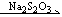 I-
I-
方法二I-(样品) I2
I2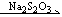 I-
I-
| A.方法二对样品所做处理操作简便,用作微量的测定更准确 |
| B.当待测液由无色变为蓝色时即达到滴定终点 |
| C.方法一与方法二测量出的样品浓度比为6:l |
| D.假设各步骤操作均得当,方法一所消耗Na2S2O3标准溶液的体积是方法二的6倍 |
D
解析试题分析: A、很难控制使Br2恰好反应,错误;B、当待测液由蓝色变为无色时即达到滴定终点,错误;C、方法一与方法二测量出的样品浓度比为1:l,错误;D、假设各步骤操作均得当,方法一中的碘单质量是方法二中的6被,所消耗Na2S2O3标准溶液的体积与方法二的6倍,正确。
考点:考查化学计算,氧化还原滴定等相关知识。

练习册系列答案
相关题目
下列叙述正确的是
| A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B.当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处 |
| C.制取并排水法收集氧气结束后,应立即停止加热 |
| D.将含硫酸的废液倒入水槽,用水冲人下水道 |
下列原理或操作不正确的是
A.在如图装置的稀硫酸中加入适量重铬酸钾或适量6%的H2O2溶液,可以使灯泡亮度增大,持续时间变长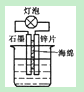 |
| B.在提纯混有少量NaCl的KNO3时,常先将混合物在较高温度下溶于水形成浓溶液,再经过冷却结晶、过滤、洗涤、干燥,获得KNO3晶体 |
| C.制摩尔盐时用酒精洗涤产品,用干净的滤纸吸干;而在制阿司匹林粗品时用冷水洗涤产品,在空气中风干 |
| D.纸层析法分离微量成份时均需有以下流程:装置制作—→点层析试样—→配制展开剂—→层析操作—→显色反应。 |
下列有关实验操作中,正确的是
| A.用试管取出试剂瓶中的NaOH溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B.银镜反应实验后的废液可先倒入水槽中,再用水冲入下水道 |
| C.向试管中滴加液体时,胶头滴管必须紧贴试管内壁,避免液体溅出 |
| D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
下列说法错误的是( )
| A.萃取操作时,选择有机萃取剂,则溶质在萃取剂的溶解度必须比水大 |
| B.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.蒸馏操作时,应使温度计水银球插入混合溶液的液面下 |
| D.配制一定物质的量浓度的溶液时,洗涤烧杯和玻璃棒的溶液必须转入容量瓶中 |
炒河虾由青色变成红色,一同学认为这种红色物质可能是河虾体内某种物质在加热的时候发生颜色的改变。就这位同学的做法而言,这应该属于科学探究步骤中的
| A.实验 | B.观察 | C.假设 | D.分类 |
实验室中以下物质的贮存方法不正确的是( )
| A.少量液溴可用水封存,防止溴挥发 |
| B.少量金属钠保存在煤油中 |
| C.浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
| D.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 |
为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是
| A.可用稀盐酸代替稀硫酸 |
| B.量气管中液体为水 |
| C.反应完全后,冷却,读取量气管体积数,再减去所加硫酸的体积,即为生成的气体体积 |
| D.实验测得该试样中碳酸氢钠质量分数偏高,可能是测定气体体积时未冷却至室温 |
