题目内容
【题目】现有金属单质A、B、C和气体乙、丙及物质D、E、F、G、H,它们之间发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
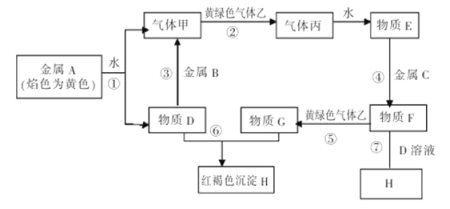
请根据以上信息回答下列问题:
(1)物质F的化学式为 。
(2)说出黄绿色气体乙的一种用途 。
(3)区别E、F两种溶液最简单的方法是 ,实验室检验G中所含的金属离子时,常在G的溶液中加入 溶液。
(4)反应①的离子方程式为 。
(5)物质F→H的转化需经过两个连续进行的反应,请写出这两个反应的化学方程式: 、 。
【答案】(1)FeCl2;(2)制取盐酸、水消毒、制取漂白粉等;
(3)滴加紫色石蕊试液,溶液变为红色就是盐酸,否则就是FeCl2;KSCN溶液
(4)2Na+2H2O=2Na++2OH-=H2↑;
(5)FeCl2+ 2NaOH=Fe(OH)2↓+2NaCl ;4Fe(OH)2 + O2+2H2O == 4Fe(OH)3 。
【解析】
试题分析:金属A焰色反应为黄色,则A是Na;Na与水反应产生的气体甲是H2,物质D是NaOH;黄绿色的气体乙是Cl2,氢气与氯气反应产生的气体丙是HCl,HCl溶于水得到溶液E是盐酸;金属B可以与NaOH反应产生氢气,则B是Al,金属C与盐酸反应产生F与氯气反应产生的G可以与NaOH溶液反应产生红褐色沉淀H,则C是Fe,F是FeCl2,G是FeCl3,H是Fe(OH)3。(1)物质F的化学式为FeCl2;(2)黄绿色气体乙是氯气,可用于制取盐酸、水消毒、制取漂白粉等;(3)E是盐酸,F是FeCl2;E、F两种溶液最简单的方法可以利用酸碱指示剂遇不同物质表现的现象。向两种溶液中分别滴加2滴紫色石蕊试液,溶液变为红色则该物质是盐酸,若不变色,就证明该溶液是FeCl2;实验室检验FeCl3中所含的金属离子时,常在G的溶液中加入KSCN溶液,若溶液变为红色,就证明含有Fe3+;(4)金属钠与水发生反应产生氢氧化钠和氢气,所以反应①的离子方程式为2Na+2H2O=2Na++2OH-=H2↑;(5)物质F→H的转化需经过两个连续进行的反应,这两个反应的化学方程式是FeCl2+ 2NaOH=Fe(OH)2↓+2NaCl ;4Fe(OH)2 + O2+2H2O == 4Fe(OH)3 。