题目内容
由原子序数依次增大的五种短周期元素A、B、C、D、E,已知A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素最高价氧化物的水化物与其氢化物反应生成一种盐;A、B、C、E四种元素分别都能与D元素形成原子个数比不相同的多种常见化合物,回答下列问题:
(1)B在周期表中的位置是 ,C元素的单质的电子式 。
(2)写出同时含A、B、C、D四种元素的一种盐的化学式 。
(3)E与D形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式为。
(4)用A和D两元素组成的单质可以制成一种燃料电池,电池中装有浓KOH溶液。用多孔的惰性电极浸入浓KOH溶液中,两极均有特制的防止气体透过的隔膜,在一极通入A的单质,另一极通入D的单质。则该电池正极的电极反应式为 。
(5)化合物C2A4和C2D4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染。已知1mol C2A4和C2D4完全反应生成两种气体时放出热量516.8KJ,则该反应的热化学方程式为 。
(1)第二周期IVA族(2分);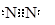 (2分);
(2分);
(2)NH4HCO3或(NH4)2CO3(2分)
(3)2Na2O2+2CO2=2Na2CO3+O2(2分)(4)O2+2H2O+4e-=4OH-(2分)
(5)2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ?H=-1033.6KJ·mol-1(2分)
解析试题分析;据题意可知A为氢原子、B为碳、 C为氮 D为氧。碳是元素周期表中的第六号元素。周期系数等于电子层数,在主族中,族系数等于最外层电子数,故(1)B的位置为第二周期IVA族。氮气有三对共用电子对,所以它的电子式为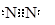 (2)据题意可知该盐为NH4HCO3或(NH4)2CO3
(2)据题意可知该盐为NH4HCO3或(NH4)2CO3
考点;考查元素周期表的相关知识以及原电池的相关知识

下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| D.Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |
下表是元素周期表的一部分,针对所给的元素,完成下列各小题。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | | | | C | N | O | |
| 3 | Na | | Al | Si | | S | Cl |
21. 第3周期中金属性最强的元素是 (填元素名称)。
22. C、N和O原子半径由小到大的顺序的是 。
23. 第3周期中气态氢化物最稳定的是 (填化学式)。
24. Si是带来人类文明的重要元素之一,其氧化物化学式是 。
25. 铝是大自然赐予人类的宝物。它的一个用途是发生铝热反应,冶炼某些难熔金属,写出
该反应的一个化学方程式 。
26. S元素形成的氢化物与其氧化物SO2相遇后的现象是 。
 C2D4(g)达到平衡状态的标志是 ;
C2D4(g)达到平衡状态的标志是 ; 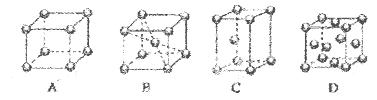
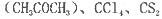 等互溶。
等互溶。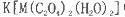 中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。
中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。