题目内容
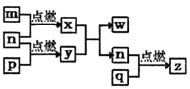
【题目】铬渣(铬主要以Cr2O3形式存在,同时含有Al2O3、SiO2等杂质)是铬电镀过程中产生的含铬污泥,实现其综合利用,可减少铬产生的环境污染。铬渣综合利用工艺流程如下:
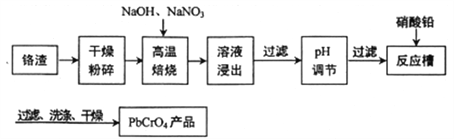
请回答下列问题:
(1)焙烧得到的产物含有Na2CrO4和一种无污染的气体,则生成Na2CrO4的反应方程式为________________________________________________________。
(2)除去铝元素的离子方程式为__________________________________________。
(3)理论上加入醋酸铅、硝酸铅均可以得到铬酸铅沉淀,工艺流程中不选用醋酸铅的原因是___________。
(4)铬酸铅是一种用于水彩和油彩的筑色颜料,遇到空气中的硫化物颜色会变黑,该过程的化学反应方程式为___________________________。
(5)实验室常利用Cr3+在碱性溶液中的还原性,使其转化为CrO42-,从而实现与Al3+的分离,这个过程中需要加入的两种试剂是__________、__________(填化学式),分离操作是_______________________。
【答案】5Cr2O3+14NaOH+6NaNO3 ==10Na2CrO4+3N2↑+7H2O AlO2-+H++H2O==Al(OH)3↓ 不引入新的杂质 PbCrO4+H2S==PbS+H2CrO4 NH3·H2O H2O2 过滤
【解析】
干燥粉碎铬渣(铬主要以Cr2O3形式存在,同时含有Al2O3、SiO2等杂质),加入NaOH、NaNO3,发生反应:5Cr2O3+14NaOH+6NaNO3![]() 10Na2CrO4+3N2↑+7H2O,浸出液含有NaOH、NaNO3、Na2CrO4、Na2SiO3、NaAlO2,除去不溶性杂质,加入硝酸调节pH,除去NaOH、Na2SiO3、NaAlO2,过滤,滤液为NaNO3、NaNO3、Na2CrO4,加入硝酸铅,得到铬酸铅沉淀,过滤、洗涤、干燥得产品,据此分析解答。
10Na2CrO4+3N2↑+7H2O,浸出液含有NaOH、NaNO3、Na2CrO4、Na2SiO3、NaAlO2,除去不溶性杂质,加入硝酸调节pH,除去NaOH、Na2SiO3、NaAlO2,过滤,滤液为NaNO3、NaNO3、Na2CrO4,加入硝酸铅,得到铬酸铅沉淀,过滤、洗涤、干燥得产品,据此分析解答。
(1)焙烧得到的产物含有Na2CrO4和一种无污染的气体氮气,则生成Na2CrO4的化学方程式为5Cr2O3+14NaOH+6NaNO3=10Na2CrO4+3N2↑+7H2O;
(2)氧化铝与氢氧化钠反应生成偏铝酸钠,通过调节pH转化为氢氧化铝沉淀,则除去铝元素的离子方程式为AlO2-+H++H2O=Al(OH)3↓;
(3)工艺流程中不选用醋酸铅的原因是不引入新的杂质;
(4)铬酸铅遇到空气中的硫化物颜色会变黑,说明有PbS产生,因此该过程的化学方程式为PbCrO4+H2S=PbS+H2CrO4;
(5)由于氢氧化铝能溶于强碱溶液中,NH3·H2O不会溶解氢氧化铝沉淀,所以加入NH3·H2O提供碱性环境,而且将Al3+转化为氢氧化铝沉淀;要转化为CrO42-,需要加入氧化剂,因此加入H2O2将Cr3+氧化为CrO42-,不会引人杂质,所以这个过程中需要加入的试剂是NH3·H2O、H2O2,分离操作是过滤。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案