题目内容
14.根据下列实验内容得出的结论正确的是( )| 选项 | 实验内容 | 结论 |
| A | 一红棕色气体能使湿润的KI-淀粉试纸变蓝 | 证明该红棕色气体一定为溴蒸气 |
| B | 向某溶液中加入氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| C | 铝箔在酒精灯火焰上加热熔化但不滴落 | 说明铝箔表面氧化铝膜熔点高于铝 |
| D | 取少量待测晶体于试管中,加浓的NaOH溶液并加热,试管口湿润的红色石蕊试纸变蓝 | 证明晶体成分中含有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化氮也能将碘离子氧化生成碘单质;
B.能和氯化钡溶液反应生成白色沉淀的离子有:硫酸根离子、亚硫酸根离子、银离子;
C.铝与氧气反应生成氧化铝的熔点高;
D.铵根离子和氢氧根离子反应生成一水合氨,一水合氨受热分解生成氨气,氨气遇湿润的红色石蕊试纸变蓝色.
解答 解:A.二氧化氮也能将碘离子氧化生成碘单质,所以该红棕色气体还可能是二氧化氮,故A错误;
B.能和氯化钡溶液反应生成白色沉淀的离子有:硫酸根离子、亚硫酸根离子、银离子,所以该溶液中不一定含有硫酸根离子,故B错误;
C.铝与氧气反应生成氧化铝的熔点高,则铝箔在酒精灯火焰上加热熔化但不滴落,故C正确;
D.铵根离子和氢氧根离子反应生成一水合氨,一水合氨受热分解生成氨气,氨气遇湿润的红色石蕊试纸变蓝色,所以取少量待测晶体于试管中,加浓的NaOH溶液并加热,试管口湿润的红色石蕊试纸变蓝,说明该晶体中含有铵根离子,故D正确;
故选CD.
点评 本题考查化学实验方案评价,为高频考点,涉及离子检验、物质检验等知识点,明确物质性质是解本题关键,知道常见离子的检验方法及现象,易错选项是B,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
4.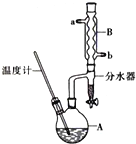 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的主要实验装置如图:反应物和产物的相关数据如下
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的主要实验装置如图:反应物和产物的相关数据如下
据如下:
合成正丁醚的步骤:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间,分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70mL水的分液漏斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为将浓H2SO4滴加到正丁醇中.
写出步骤②中制备正丁醚的化学方程式2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O.
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O.
(2)加热A前,需先从b(填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓H2SO4,振摇后静置,粗产物应从分液漏斗的上(填“上”或“下”)口分离出.
(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐Na2SO4.
(5)步骤⑤中,加热蒸馏时应收集d(填选项字母)左右的馏分.
a.100℃b. 117℃c. 135℃d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.(填物质名称)
(7)本实验中,正丁醚的产率为33.85%.
 正丁醚常用作有机反应的溶剂.实验室制备正丁醚的主要实验装置如图:反应物和产物的相关数据如下
正丁醚常用作有机反应的溶剂.实验室制备正丁醚的主要实验装置如图:反应物和产物的相关数据如下据如下:
| 相对分 子质量 | 沸点/ ℃ | 密度 (g•cm-3) | 水中溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间,分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70mL水的分液漏斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为将浓H2SO4滴加到正丁醇中.
写出步骤②中制备正丁醚的化学方程式2CH3CH2CH2CH2OH
 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O.
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O. (2)加热A前,需先从b(填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去浓H2SO4,振摇后静置,粗产物应从分液漏斗的上(填“上”或“下”)口分离出.
(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐Na2SO4.
(5)步骤⑤中,加热蒸馏时应收集d(填选项字母)左右的馏分.
a.100℃b. 117℃c. 135℃d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为正丁醇,下层液体的主要成分为水.(填物质名称)
(7)本实验中,正丁醚的产率为33.85%.
5.下列反应的离子方程式正确且表示复分解反应的是( )
| A. | 钠跟水的反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| C. | 碳酸氢钙溶液加入过量的氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 碳酸氢钠溶液中加入盐酸:HCO3-+H+═CO2↑+H2O |
2.用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.2000mol•L-1的氢氧化钠溶液(指示剂为酚酞)滴定得结果如下:
(1)达到滴定终点的时溶液颜色的变化为无色到浅红色;
(2)根据以上数据可以计算出盐酸的物质的量浓度为0.1448mol/L;
(3)以下操作造成测定结果偏高的原因可能是CD.
A、滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B、盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C、滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D、未用标准液润洗碱式滴定管.
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.40mL | 18.50mL |
| 第二次 | 1.30mL | 18.05mL |
| 第三次 | 3.10mL | 21.20mL |
(2)根据以上数据可以计算出盐酸的物质的量浓度为0.1448mol/L;
(3)以下操作造成测定结果偏高的原因可能是CD.
A、滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B、盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C、滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D、未用标准液润洗碱式滴定管.
19.在某无色透明的碱性溶液中,能共存的离子组是( )
| A. | Na+、K+、SO42-、HCO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Fe3+、K+、SO42-、Cl- | D. | Na+、K+、Cl-、NO3- |
6.下列有机物的命名正确的是( )
| A. | 1-甲基戊烷 | B. | 2,3-二甲基戊烷 | C. | 3-戊烯 | D. | 3,4-二甲基戊烷 |
3.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 25℃时,0.1mol/L的 pH=4.5的NaHC2O4溶液:c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| B. | 25℃时,pH=9、浓度均为0.1 mol/L的NH3•H2O和NH4Cl混合溶液:c(NH4+)+c(H+)>c(NH3•H2O)+c(OH-) | |
| C. | NaHCO3溶液:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| D. | 0.1mol/L(NH4)2Fe(SO4)2溶液中:c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) |
4.下列说法正确的是( )
| A. | 水俣病是因为长期食用富含汞的鱼和贝类而造成的慢性汞中毒 | |
| B. | 水俣病是长期食用含镉的污水灌溉的水稻造成的 | |
| C. | 日本的水俣病是有机汞引起的汞中毒 | |
| D. | 深海的生物对重金属离子的富集浓度大 |