题目内容
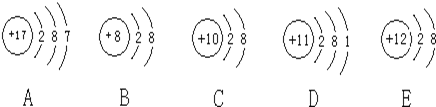
【题目】A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同。A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)A元素单质的化学式为__________________。
(2)由A、B、C三种元素形成的化合物的电子式为___________,这种化合物形成的晶体中所含的化学键类型有______________。
(3)A、B、D三种元素形成的一种化合物和A、B形成的一种化合物能发生氧化还原反应,反应的化学方程式为_____________________________________________。
(4)B、C、E三种元素形成一种盐,此盐中三种原子个数比为1∶1∶1,在25℃时,将该盐溶于水,测得溶液pH>7,理由是___________________________(用离子方程式表示)。
【答案】H2 ![]() 离子键、共价键 H2SO3 +H2O2=H2SO4 +H2O ClO-+H2O =HClO+OH-
离子键、共价键 H2SO3 +H2O2=H2SO4 +H2O ClO-+H2O =HClO+OH-
【解析】
A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,则A为H元素;因A与C、B与D分别为同主族,则C为Na元素;AE是18e-的化合物,则E为Cl元素;又因为B与C的最外层电子数之和与E的最外层电子数相同,则B最外层电子数=7-1=6,则B为O元素,D为S元素,据此解答。
A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,则A为H元素;因A与C、B与D分别为同主族,则C为Na元素;AE是18e-的化合物,则E为Cl元素;又因为B与C的最外层电子数之和与E的最外层电子数相同,则B最外层电子数=7-1=6,则B为O元素,D为S元素,
(1)A元素单质的化学式为H2;
(2)由H、O、Na三种元素形成的化合物为NaOH,其电子式为![]() ,晶体中所含的化学键有:离子键、共价键;
,晶体中所含的化学键有:离子键、共价键;
(3)H、O、S三种元素形成的一种化合物和H、O形成的一种化合物能发生氧化还原反应,应是亚硫酸与过氧化氢反应生成硫酸、水,反应的化学方程式为:H2SO3+H2O2═H2SO4+H2O;
(4)O、Na、Cl三种元素形成一种盐,此盐中三种原子个数比为1:1:1,则该盐为NaClO,在25℃时,将该盐溶于水,溶液中ClO-水解:ClO-+H2OHClO+OH-,破坏水的电离平衡,溶液呈碱性,即溶液的pH>7。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案