题目内容
【题目】能源危机是当前一个全球性问题。请回答下列问题:
(1)下列做法有助于能源“开源节流”的是_____________(填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)甲烷是一种优良的气体燃料。已知1g 甲烷完全燃烧生成CO2和H2O(l)过程中,放出55.6kJ 热量,写出表示甲烷燃烧热的热化学方程式:____________________________。
(3)已知稀溶液中,含30g溶质的醋酸溶液与NaOH 溶液恰好完全反应时,放出28.55kJ热量。写出表示醋酸与NaOH 反应的中和热的热化学方程式:___________________。
(4)已知: CH4(g)+2O2(g) =CO2(g)+2H2O(l) △H=-890.3kJmol-1
N2(g)+O2(g) ==2NO(g) △H=+180kJmol-1
CH4 可用于脱硝,其热化学方程式为CH4(g)+4NO(g)==CO2(g)+2N2(g)+2 H2O(l) △H=__________。
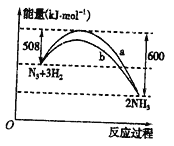
(5)如下图是298 K时N2与H2反应过程中能量变化的曲线图,该反应的热化学方程式为:_____________________________。
(6)已知断裂下列化学键需要吸收的能量分别为: H-H a kJmol-1\、H-O b kJmol-1、O=O c kJmol-1,根据有关数据估算氢气与氧气的反应:2H2+O2=2H2O 该反应的△H=_________________。
【答案】 ac CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-889.6kJ·mol-1 CH3COOH(aq) +NaOH(aq)=CH3COONa(aq)+H2O △H= -57.1kJ·mol-1 -1250.3 kJ·mol-1 N2(g)+2H2(g)=2NH3(g) △H=-92kJ·mol-1 (2a+c-4b)kJ·mol-1
【解析】本题主要考查反应热的计算。
(1)a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源,有助于能源“开源节流”;b.大力开采煤、石油和天然气以满足人们日益增长的能源需求,不利于能源“开源节流”;c.减少资源消耗,注重资源的重复使用、资源的循环再生,有助于能源“开源节流”。故选ac。
(2)16g即1mol甲烷完全燃烧生成CO2和H2O(l)过程中,放出889.6kJ热量,表示甲烷燃烧热的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-889.6kJ·mol-1。
(3)含30g即0.5mol溶质的醋酸溶液与NaOH 溶液恰好完全反应时,放出28.55kJ热量,表示醋酸与NaOH 反应的中和热的热化学方程式:CH3COOH(aq) +NaOH(aq)=CH3COONa(aq)+H2O △H= -57.1kJ·mol-1。
(4)将上述两个热化学方程式的反应热分别表示为△H1、△H2,△H=△H1-2△H2= -1250.3kJ·mol-1。
(5)△H=(508-600)KJ·mol-1=-92kJ·mol-1,该反应的热化学方程式为:N2(g)+2H2(g)=2NH3(g) △H=-92kJ·mol-1。
(6)△H=反应物键能之和-生成物键能之和=(2a+c-4b)kJ·mol-1。