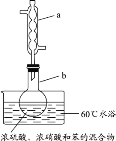
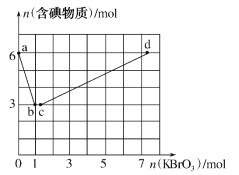
题目内容
【题目】氨气是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:CO+2H2![]() CH3OH(g)。该可逆反应达到平衡的标志是________。
CH3OH(g)。该可逆反应达到平衡的标志是________。
A.2 v正(H2)= v逆(CH3OH)
B.单位时间生成m molCO的同时生成2m molH2
C.容器内气体的平均相对分子质量不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取化工原料气氢气,某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据。
时间/min | CH4(mol) | H2O(mol) | CO(mol) | H2(mol) |
0 | 0.40 | 1.00 | 0 | 0 |
5 | a | 0.80 | c | 0.60 |
7 | 0.20 | b | 0.20 | d |
10 | 0.21 | 0.81 | 0.19 | 0.64 |
请回答下列问题:
①该温度下,上述反应的平衡常数K=________;
②反应在7~10min内,CO的物质的量减少的原因可能是____________(填字母)。
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时,上述反应向_____(填“正反应”或“逆反应”)方向进行。若要使上述反应开始时向逆反应方向进行,则a的取值范围为__________。
【答案】C 0.0675 D 正反应 a>0.26
【解析】
⑴A. 2 v正(H2)= v逆(CH3OH),一个正向一个逆向,两个相反方向,反速率比不等于计量系数比,不能作为平衡的标志;B. 单位时间生成m molCO的同时生成2m molH2,都是逆向,因此不能作为判断平衡标志;C. 平均相对分子质量等于气体质量除以物质的量,气体物质的量减小,平均相对分子质量增大,当容器内气体的平均相对分子质量不再变化,则达到平衡;D. 混合气体密度等于气体质量除以容器体积,气体质量不变,容器体积不变,混合气体的密度始终不变,不能作为判断平衡标志。
⑵①根据反应方程CH4(g) + H2O(g) ![]() CO(g) + 3H2(g),计算7min时CH4的物质的量并得到n(H2O),说明在5min时已达到平衡,再计算出n(CO)、n(H2),再计算反应的平衡常数;②A. 减少CH4的物质的量,平衡逆向移动,最终CH4的物质的量减少;B.降低温度、C. 升高温度,该反应不清楚放热还是吸热反应,因此不清楚平衡移动,而且CO在减少,H2在增加,不可能是温度改变;D. 充入H2,平衡逆向移动,CO量减少,H2的物质的量比原来多;③利用浓度商与平衡常数大小判断反应向哪个方向进行,利用浓度商与平衡常数计算开始时向逆反应方向进行a的取值范围。
CO(g) + 3H2(g),计算7min时CH4的物质的量并得到n(H2O),说明在5min时已达到平衡,再计算出n(CO)、n(H2),再计算反应的平衡常数;②A. 减少CH4的物质的量,平衡逆向移动,最终CH4的物质的量减少;B.降低温度、C. 升高温度,该反应不清楚放热还是吸热反应,因此不清楚平衡移动,而且CO在减少,H2在增加,不可能是温度改变;D. 充入H2,平衡逆向移动,CO量减少,H2的物质的量比原来多;③利用浓度商与平衡常数大小判断反应向哪个方向进行,利用浓度商与平衡常数计算开始时向逆反应方向进行a的取值范围。
⑴A. 2 v正(H2)= v逆(CH3OH),一个正向一个逆向,两个相反方向,反速率比不等于计量系数比,不能作为平衡的标志,故A不符合题意;B. 单位时间生成m molCO的同时生成2m molH2,都是逆向,因此不能作为判断平衡标志,故B不符合题意;C. 平均相对分子质量等于气体质量除以物质的量,气体物质的量减小,平均相对分子质量增大,当容器内气体的平均相对分子质量不再变化,则达到平衡,故C符合题意;D. 混合气体密度等于气体质量除以容器体积,气体质量不变,容器体积不变,混合气体的密度始终不变,不能作为判断平衡标志,故D不符合题意;综上所述,答案为C。
⑵①根据反应方程CH4(g) + H2O(g) ![]() CO(g) + 3H2(g),7min时CH4的物质的量为0.2mol,Δn(CH4) = 0.2mol,Δn(H2O) = 0.2mol,Δn(CO) = 0.2mol,则n(H2O) = 0.8mol,说明在5min时已达到平衡,n(CO) = 0.2mol,n(H2) = 0.6mol,该温度下,上述反应的平衡常数
CO(g) + 3H2(g),7min时CH4的物质的量为0.2mol,Δn(CH4) = 0.2mol,Δn(H2O) = 0.2mol,Δn(CO) = 0.2mol,则n(H2O) = 0.8mol,说明在5min时已达到平衡,n(CO) = 0.2mol,n(H2) = 0.6mol,该温度下,上述反应的平衡常数 ;故答案为:0.0675。
;故答案为:0.0675。
②A. 减少CH4的物质的量,平衡逆向移动,最终CH4的物质的量减少,故A不符合题意;B.降低温度、C. 升高温度,该反应不清楚放热还是吸热反应,因此不清楚平衡移动,而且CO在减少,H2在增加,不可能是温度改变,故B、C不符合题意;D. 充入H2,平衡逆向移动,CO量减少,H2的物质的量比原来多,故D符合题意;综上所述,答案为D。
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时, ,因此上述反应向正反应方向进行。若要使上述反应开始时向逆反应方向进行,
,因此上述反应向正反应方向进行。若要使上述反应开始时向逆反应方向进行, ,则a的取值范围为a>0.26。
,则a的取值范围为a>0.26。

 阅读快车系列答案
阅读快车系列答案【题目】(1)工业上制取纯净的CuCl2·2H2O的主要过程是
①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;
②对①所得滤液按下列步骤进行操作:
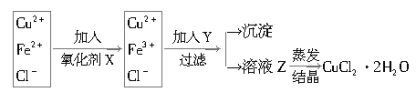
已知:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp/25 ℃ mol3·L-3 | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
请回答下列问题:
①加入的氧化剂X,下列物质最好选用的是 ______ .
A.KMnO4 B.H2O2 C.氯水D.HNO3
②加入Y的作用是___________________________,Y的化学式为____________。
③溶液乙在蒸发结晶时应注意:________________________________。
(2)如图为相互串联的甲、乙两个电解池,试回答下列问题:
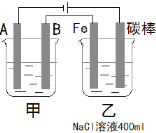
甲池若为用电解原理精炼铜的装置,阴极增重19.2 g,则乙池阳极放出气体在标准状况下的体积为__________L(不考虑气体的溶解情况)
【题目】氮的化合物在相互转化、工业生产等方面应用广泛,回答下列问题。
(1)N2O是一种能刺激神经使人发笑的气体,可发生分解反应2N2O=2N2+O2,碘蒸气能大幅度提高N2O的分解速率,反应历程为:
第一步: I2(g)=2I(g) (快反应)
第二步: I(g)+N2O(g)=N2(g)+IO(g) (慢反应)
第三步: IO(g)+N2O(g)=N2(g)+O2(g)+I(g) (快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_____(填标号)。
A.温度升高,该反应速率常数k值增大
B.第三步对总反应速率起决定作用
C.第二步活化能比第三步大
D.I2作催化剂,其浓度大小与N2O分解速率无关
(2)温度为T1时,在二个容积均为1L的密闭容器中仅发生反应:2NO(g)+O2(g)![]() 2NO2(g) △H<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数。
2NO2(g) △H<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数。
容器编号 | 起始浓度/ mol·L-1 | 平衡浓度/ mol·L-1 | ||
c(NO) | c(O2) | c(NO2) | c(O2) | |
Ⅰ | 0.6 | 0.3 | 0 | 0.2 |
Ⅱ | 0.3 | 0.25 | 0.2 | |
①温度为T1时,![]() =________;当温度升高为T2时,k正、k逆分别增大m倍和n倍,则m______n(填“>”“<”或“=”)。
=________;当温度升高为T2时,k正、k逆分别增大m倍和n倍,则m______n(填“>”“<”或“=”)。
②容器Ⅱ中起始时v正_____v逆(填“>”“<”或“=”),理由是_______。
(3)NH3与CO2反应可合成尿素[化学式为CO(NH2)2],反应方程式为2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)在合成塔中进行,下图中Ⅰ、Ⅱ、Ⅲ三条曲线分别表示温度为T℃时,按不同氨碳比
CO(NH2)2(l)+H2O(g)在合成塔中进行,下图中Ⅰ、Ⅱ、Ⅲ三条曲线分别表示温度为T℃时,按不同氨碳比![]() 和水碳比
和水碳比![]() 投料时,二氧化碳平衡转化率的情况。
投料时,二氧化碳平衡转化率的情况。
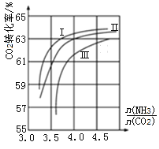
①曲线Ⅰ、Ⅱ、Ⅲ中水碳比的数值分别为0.6~0.7,1~1.1,1.5~1.6,则生产中应选用的水碳比数值范围是______。
②在选择氨碳比时,工程师认为控制在4.0左右比较适宜,不选择4.5,理由是_____。