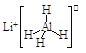题目内容
【题目】我国科学家设计出一种可将光能转化为电能和化学能的天然气脱硫装置,如图,利用该装置可实现:H2S+O2 ═H2O2 +S。已知甲池中发生转化: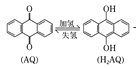 。下列说法错误的是
。下列说法错误的是
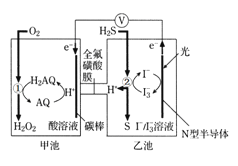
A.甲池碳棒上发生电极反应:AQ+2H++2e-=H2AQ
B.该装置工作时,溶液中的H+从甲池经过全氟磺酸膜进入乙池
C.甲池①处发生反应:O2+H2AQ=H2O2+AQ
D.乙池②处发生反应:H2S+I3-=3I-+S↓+2H+
【答案】B
【解析】
A.由装置图可知,甲池中碳棒上发生得电子的还原反应,电极反应为AQ+2H++2e-=H2AQ,故A不符合题意;
B.原电池中阳离子移向正极,甲池中碳棒是正极,所以溶液中的H+从乙池经过全氟磺酸膜进入甲池,故B符合题意;
C.甲池①处发生O2和H2AQ反应生成H2O2和AQ,方程式为O2+H2AQ=H2O2+AQ,故C不符合题意;
D.乙池②处,硫化氢失电子生成硫单质,![]() 得电子生成I-,离子方程式为:H2S+
得电子生成I-,离子方程式为:H2S+![]() =3I-+S↓+2H+,故D不符合题意;
=3I-+S↓+2H+,故D不符合题意;
故选:B。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】CH4-CO2催化重整时发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
2CO(g)+2H2(g),不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)某温度下,向1L的密闭容器中充入0.2molCH4与0.1molCO2,发生CH4-CO2催化重整反应,10min时达到平衡,测得平衡混合物中CO(g)的体积分数为20%,则用CH4表示的反应速率为______,CO2的平衡转化率为______。
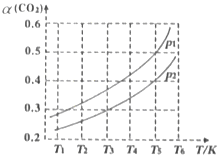
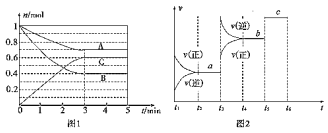
(2)若CO2的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。由图可知:压强p1______p2(选填“>“、“<“或“=”),理由是______。
(3)在一定温度下,向固定容积为2L的密闭容器中充入0.1moCH4与0.1mo1CO2发生CH4-CO2催化重整反应,达平衡时CO2的平衡转化率为50%,则此条件下该反应的平衡常数为K=______;平衡后保持温度不变,若再充入0.15molCH4、0.15molCO2、0.1molCO、0.1molH2,则此时v正______(选填“>”、“<”或“=”)v逆。
(4)已知:C(s)+2H2(g)=CH4(g)△H1=-75 kJmol-1
C(s)+O2(g)=CO2(g)△H2=-394 kJmol-1
C(s)+![]() O2(g)=CO(g)△H3=-111 kJmol-1
O2(g)=CO(g)△H3=-111 kJmol-1
①催化重整反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)的△H=______kJmol-1。
2CO(g)+2H2(g)的△H=______kJmol-1。
②反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
积碳反应CH4(g)=C(s)+2H2(g) | 消碳反应CO2(g)+C(s)=CO(g) | ||
△H/(kJmol-1) | 75 | 172 | |
活化能/(kJmol-1) | 催化剂X | 33 | 91 |
催化剂Y | 43 | 72 | |
由上表判断,催化剂X______Y(填“优于”或“劣于”),理由是______。
【题目】在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2CuCl+2CO+2H2O=Cu2Cl22CO2H2O。
回答下列问题:
(1)Cu在元素周期表中属于______(选填“s”、“p”、“d”或“ds”)区元素。研究人员发现在高温超导材料镧钡铜氧化物中含有Cu3+,基态Cu3+的电子排布式为______。
(2)C、N、O三种原子中的第一电离能最大的是______。NO3-离子的空间构型是______。
(3)CO与N2互称等电子体。
①它们的分子中都存在三个共价键,其中包含______个σ键,______个π键。
②下表为CO和N2的有关信息。
键的类型 | A-B(单键) | A=B(双键) | A≡B(叁键) | |
键能(kJ/mol) | CO | 351 | 803 | 1071 |
N2 | 159 | 418 | 946 | |
根据表中数据,说明CO比N2活泼的原因是______。
(4)Cu2Cl22CO2H2O是一种配合物,其结构如图所示:
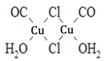
①该配合物中氯原子的杂化方式为______。
②该配合物中,CO作配体时配位原子是C而不是O的原因是______。
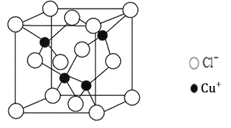
(5)阿伏加德罗常数的测定有多种方法,X射线衍射法就是其中的一种。通过对CuCl晶体的X射线衍射图象分析,可以得出CuCl的晶胞如图所示,则距离每个Cu+最近的Cl-的个数为______。若晶体中Cl-呈立方面心最密堆积方式排列,Cl-的半径为a pm,晶体的密度为ρg/cm3,阿伏加德罗常数NA=______(列计算式表达)。