题目内容
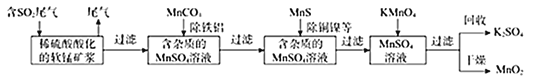
【题目】某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂。通过如下简化流程既脱除燃媒尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
请回答下列问题:
(1)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是______(填编号);
A.NaOH溶液、酚酞溶液 B.稀H2SO4酸化的KMnO4溶液 C.碘水、淀粉溶液 D.氨水、酚酞溶液
(2)写出软锰矿浆吸收SO2的化学方程式______;
(3)用MnCO3,能除去溶液中的Al3+和Fe3+,用原理解释:______。
(4)写出KMnO4与MnSO4溶液反应的离子方程式______;
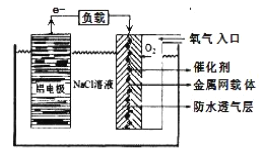
(5)工业上将K2MnO4溶液采用惰性电极隔膜法电解,可制得KMnO4.装置如图:
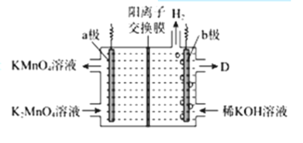
①D是溶液______;
②结合电极反应式简述生成KMnO4的原理:______;
(6)除杂后得到的MnSO4溶液可以通过______(填操作名称)、过滤制得硫酸锰晶体。
【答案】BC MnO2+SO2=MnSO4 消耗溶液中氢离子,促进Al3+和Fe3+水解生成氢氧化物沉淀 2MnO4-+3Mn2++2H2O=5MnO2+4H+ 浓KOH溶液 a极上发生MnO42--e-═MnO4-,部分钾离子通过阳离子交换膜进入阴极区,阳极区生成KMnO4 蒸发浓缩、冷却结晶
【解析】
由流程可知,含二氧化硫的尾气通入稀硫酸酸化的软锰矿浆中,二氧化硫能被二氧化锰氧化为硫酸锰,MnCO3能除去溶液中Al3+和Fe3+,MnS能将铜、镍离子还原为单质,高锰酸钾能与硫酸锰反应生成二氧化锰,通过过滤获得二氧化锰、硫酸钾。
(1)二氧化硫可被高锰酸钾、碘水氧化,根据颜色变化,可准确判断滴定终点,从而准确测定其含量,而与碱反应时选酚酞作指示剂,吸收不彻底,不能准确测定二氧化硫的含量。答案为:BC;
(2)锰矿浆吸收SO2,生成硫酸锰,反应的化学方程式为MnO2+SO2=MnSO4。答案为:MnO2+SO2=MnSO4;
(3)在水溶液中,Al3+和Fe3+都能水解生成H+,MnCO3能与H+反应从而促进Al3+和Fe3+完全转化为氢氧化物沉淀,从而除去溶液中的Al3+和Fe3+。用原理解释为消耗溶液中氢离子,促进Al3+和Fe3+水解生成氢氧化物沉淀。答案为:消耗溶液中氢离子,促进Al3+和Fe3+水解生成氢氧化物沉淀;
(4)KMnO4与MnSO4溶液发生归中反应,生成MnO2沉淀,反应的离子方程式为2MnO4-+3Mn2++2H2O=5MnO2↓+4H+。答案为:2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;
(5)①由图可知,a电极上MnO42-失去电子,b电极上水电离出的氢离子得到电子生成OH-,左侧溶液中的K+通过阳离子交换膜进入右侧溶液,所以右侧KOH的浓度变大,D是浓KOH溶液。答案为:浓KOH溶液;
②a为阳极,阳极上K2MnO4失去电子发生氧化反应,电极反应式为MnO42--e-═MnO4-,部分钾离子通过阳离子交换膜进入阴极区,阳极区生成KMnO4。答案为:a极上发生MnO42--e-═MnO4-,部分钾离子通过阳离子交换膜进入阴极区,阳极区生成KMnO4;
(6)由MnSO4溶液得到MnSO4H2O晶体,应蒸发浓缩、冷却结晶、过滤及干燥。答案为:蒸发浓缩、冷却结晶。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】化学反应速率和化学反应的限度是化学反应原理的重要组成部分。
(1)探究反应条件对0.10mol/LNa2S2O3溶液与0.10mol/L 稀H2SO4反应速率的影响。反应方程式为:Na2S2O3 +H2SO4=Na2SO4+S↓+SO2↑+H2O。设计测定结果如下:
编号 | 反应温度/℃ | Na2S2O3溶液/mL | 甲/mL | H2SO4溶液/mL | 乙 |
① | 25 | 10.0 | 0 | 10.0 | x |
② | 25 | 5.0 | A | 10.0 | y |
③ | 0 | 10.0 | 0 | 10.0 | z |
若上述实验①②是探究浓度对化学反应速率的影响,则a为____________,乙是实验需要测量的物理量,则表格中“乙”为____________,x、y、z的大小关系是____________。
(2)氨气具有广泛的用途,工业上合成氨的反应是N2(g)+3H2(g)=2NH3(g).
①已知:
化学键 | H-H | N≡N | N-H |
键能kJ/mol(断开1mol化学键所需要的能量) | 436 | 945 | 391 |
则合成氨的热化学方程式是________________________________________。
②若反应起始时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L,达到平衡时NH3浓度的范围是____________________。
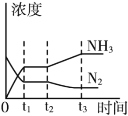
③如图表示该反应在t1时刻达到化学平衡,在t2时因改变某个条件而发生变化的情况,则t2时刻改变条件可能是__________。
【题目】表为元素周期表的一部分,表中a-f代表六种短周期主族元素,完成下列填空:
a | b | c |
d | e | f |
(1)六种元素中,原子半径最大的是_____________(填元素编号)。
(2)若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是________;六种元素中,最高价氧化物对应水化物的酸性最强的是_________(填元素符号)
(3)若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性___________(选填“强”、“弱”)
(4)若b为非金属元素,则以下推断正确的是___________(选填编号)。
①a一定是金属元素 ②d一定是金属元素 ③f一定是非金属元素