题目内容
在水的电离平衡中,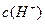 和
和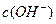 的关系如下图所示:
的关系如下图所示:
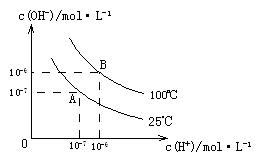
(1)A点水的离子积为1×10-14,B点水的离子积为 。造成水的离子积变化的原因是 。
(2)25℃时,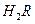 在水溶液中的电离方程式为:
在水溶液中的电离方程式为:
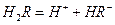 ,
,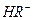

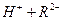 。
。
① 0.1 mol/L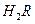 溶液的pH 1(填“>”、“<”或“=”)。
溶液的pH 1(填“>”、“<”或“=”)。
②在0.1 mol/L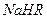 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:
。
(3)100℃时,0.01 mol/L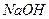 溶液的pH = 。
溶液的pH = 。
(4)100℃时,将pH =8的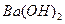 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则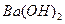 溶液与盐酸的体积比为 。
溶液与盐酸的体积比为 。
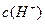 和
和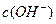 的关系如下图所示:
的关系如下图所示:
(1)A点水的离子积为1×10-14,B点水的离子积为 。造成水的离子积变化的原因是 。
(2)25℃时,
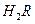 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: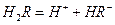 ,
,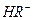

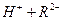 。
。① 0.1 mol/L
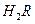 溶液的pH 1(填“>”、“<”或“=”)。
溶液的pH 1(填“>”、“<”或“=”)。②在0.1 mol/L
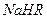 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:。
(3)100℃时,0.01 mol/L
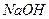 溶液的pH = 。
溶液的pH = 。(4)100℃时,将pH =8的
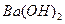 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则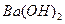 溶液与盐酸的体积比为 。
溶液与盐酸的体积比为 。(1) ; 水的电离要吸热,温度升高,水的电离程度增大,即离子积增大。
; 水的电离要吸热,温度升高,水的电离程度增大,即离子积增大。
(2)① < ②
(3)10 (4)2:9 (每空2分)
 ; 水的电离要吸热,温度升高,水的电离程度增大,即离子积增大。
; 水的电离要吸热,温度升高,水的电离程度增大,即离子积增大。(2)① < ②

(3)10 (4)2:9 (每空2分)
略

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
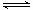 2HI(g);(正反应放热),当达到平衡后,t0时改变反应的某一条件(混合气体总物质的量不变),且造成容器内压强增大,下列说法正确的是( )
2HI(g);(正反应放热),当达到平衡后,t0时改变反应的某一条件(混合气体总物质的量不变),且造成容器内压强增大,下列说法正确的是( )
 2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率)
2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率) 


 点KW间的关系:B>C>A=D=E
点KW间的关系:B>C>A=D=E C(g)+D(g)在一定条件下已达到化学平衡状态的事实是。
C(g)+D(g)在一定条件下已达到化学平衡状态的事实是。  CO(g) + H2(g)
CO(g) + H2(g) 2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示。下列说法正确的是
2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示。下列说法正确的是