题目内容
在aLAl2(SO4)3和(NH4)2SO4的混合物溶液中加入b molBaCl2,恰好使溶液中的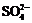 离子完全沉淀;如加入足量强碱并加热可得到c molNH3气,则原溶液中的Al3+离子浓度(mol/L)为( )
离子完全沉淀;如加入足量强碱并加热可得到c molNH3气,则原溶液中的Al3+离子浓度(mol/L)为( )
A.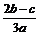 | B.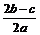 | C.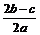 | D.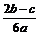 |
A
解析试题分析:设Al2(SO4)3、(NH4)2SO4的物质的量分别为xmol、ymol该过程发生的反应有:
Al2(SO4)3+3BaCl2=2AlCl3+3BaSO4↓ (NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl
x 3x y y 2y
NH4++OH- NH3↑+H2O
NH3↑+H2O
2y 2y
得关系式:①3x+y="b" mol ②2y="c" mol。解得:x=mol y=c/2mol
故c(Al3+)="2×" [b-(c/2)]/3×a=(2b-c)/3amol/L,A正确。
考点:化学计算

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
若NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.22 g乙醛中含有3 NA个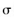 键 键 |
| B.lmol C12与足量Fe完全反应,反应中转移3 N A个电子 |
C.对于Si+O2 SiO2,每当形成2 NA个Si-O键,需断开NA个Si--Si键 SiO2,每当形成2 NA个Si-O键,需断开NA个Si--Si键 |
| D.氯元素的某种核素的质量为ag,该核素的摩尔质量为aNAg/mol |
以NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA |
| B.28gCO中所含的原子数为2NA |
| C.1L 0.1mol/LNa2CO3溶液中,含有CO32— 数为0.1NA |
| D.22.4LH2的分子数为NA |
下列化学用语正确的是
| A.乙醇的结构筒式:C2H6O |
B.CH4的比例模型: |
C.工业上制取粗硅的化学方程式:SiO2+C Si+CO2↑ Si+CO2↑ |
| D.电解饱和食盐水的离子方程式:Cl-+2H2O=Cl2↑+2OH-+H2↑ |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.NA个N2分子与0.5 NA个H2分子所占的体积比一定是2 : 1 |
| B.相同物质的量的OH-和CH3+含有相同数目的电子 |
| C.25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA |
| D.常温常压下,NO2与足量H2O反应生成0.1molNO,则转移的电子数为0.2NA |
设阿伏加德罗常数为NA,下列说法正确的是
| A.在1L1mol?L-1的盐酸溶液中含有NA个HCl分子 |
| B.假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA |
| C.标准状况下,11.2 L CCl4中含有的C—Cl 键的个数为2NA |
| D.46gNO2和N2O4混合气体降温到标况,其中含有原子总数为3NA |
设NA代表阿伏加德罗常数的数值,则下列说法正确的是
| A.1.8 g D2O含有NA个中子 |
| B.用5 mL 3 mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
| C.在Na2O2与CO2的反应中,每转移NA个电子时,消耗22.4 L的CO2 |
| D.25℃时,7 g C2H4和C3H6的混合气体中,含有NA个C-H键 |
科学家在利用无土栽培培养一些名贵花卉时,培养液中添加了多种必需元素,其配方如下,其中植物根吸收最少的离子是( )。
| 离子 | K+ | Mg2+ | Ca2+ | NO3- | H2PO4- | SO42- | Zn2+ |
 | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
A.Zn2+ B.SO42- C.Ca2+ D.H2PO4-
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA |
| B.78 g苯含有CC双键的数目为3NA |
| C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA |
| D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA |