��Ŀ����
����Ŀ���ҹ�����Ϊ��������ȱ�������涨��ʳ���б�����������ĵ��ᡣ����ʳ�����Ƿ�ӵ������������·�Ӧ��KIO3+ 5 KI+ 3H2SO4�T3K2SO4+ 3I2 + 3H2O
��1���÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ__________��
��2����˫���ű�ʾ����ת�Ʒ������Ŀ___________________��
��3�������Ӧ��ת��0.5mol���ӣ�������I2�����ʵ���Ϊ_________��
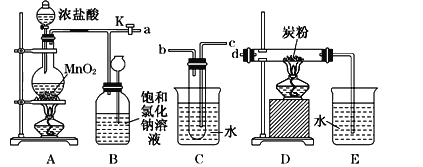
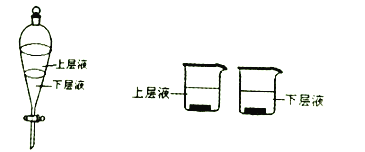
��4����Ҫ��ȡ���ɵĵ⣬���õ���ȡ��������________������ţ���
��ˮ �ھƾ� �۵�����Һ �����Ȼ�̼
���𰸡� 1��5  0.3 mol ��
0.3 mol ��
��������(1)KIO3Ϊ��������KIΪ��ԭ��,�ɷ���ʽ����֪���������ͻ�ԭ�������ʵ���֮��Ϊ1��5������:1��5 ;
��2��������ԭ��ӦKIO3+5KI+3H2SO4�T3K2SO4+3I2+3H2O�У�����ת��������£� ��Ϊ��
���� ��
��
(3)��������Ӧ����ת��5mol�������ɵⵥ�ʵ�����3mol,���������Ӧ��ת��0.5 mol����,������ I2�����ʵ���Ϊ0.3 mol,��Ϊ��0.3 mol
��4�������л���Һ�е��ܽ��Զ������ˮ�е��ܽ�������Բ�����ȡ�ķ�����ȡ��������ѡ�����Ȼ�̼����ȡ����Ϊ����.

��ϰ��ϵ�д�
 �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
�����Ŀ