题目内容
18.在下列反应中,光照对反应几乎没有影响的是( )| A. | 氯气与氢气的反应 | B. | 氯气与甲烷的反应 | ||
| C. | 氟气与氢气的反应 | D. | 次氯酸的分解 |
分析 氯气与氢气反应条件为光照或者点燃,氯气与甲烷反应条件为光照,氟气与氢气在阴暗处就能发生爆炸,次氯酸见光分解,据此解答.
解答 解:氯气与氢气反应条件为光照或者点燃,氯气与甲烷反应条件为光照,氟气与氢气在阴暗处就能发生爆炸,次氯酸见光分解,所以光照对反应几乎没有影响的是氢气与氟气的反应,
故选:C.
点评 本题考查了反应条件的选择,熟悉氯气、氟气的性质是解题关键,侧重考查学生对基础知识掌握的熟练程度,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.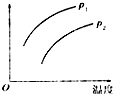 在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)?2C(g)△H>0.平衡移动关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)?2C(g)△H>0.平衡移动关系如图所示.下列说法正确的是( )
 在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)?2C(g)△H>0.平衡移动关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)?2C(g)△H>0.平衡移动关系如图所示.下列说法正确的是( )| A. | P1<P2,纵坐标表示A的质量分数 | |
| B. | P1<P2,纵坐标表示混合气体的平均摩尔质量 | |
| C. | P1<P2,纵坐标表示A的转化率 | |
| D. | P1<P2,纵坐标表示C的质量分数 |
9.已知25℃、101kPa条件下:
①4Al(s)+3O2(g)=2Al2O3(s);△H=-2834.9kJ/mol;
②4Al(s)+2O3(g)=2Al2O3(s);△H=-3119.1kJ/mol.由此得出的正确结论是( )
①4Al(s)+3O2(g)=2Al2O3(s);△H=-2834.9kJ/mol;
②4Al(s)+2O3(g)=2Al2O3(s);△H=-3119.1kJ/mol.由此得出的正确结论是( )
| A. | 等质量的O2比O3的能量低,由O2变O3为放热反应 | |
| B. | 等质量的O2比O3的能量高,由O2变O3为吸热反应 | |
| C. | O2比O3稳定,3O2(g)═2O3(g)△H=-284.2 kJ/mol | |
| D. | O2比O3稳定,3O2(g)═2O3(g)△H=+284.2 kJ/mol |
6.下列化学方程式错误的是( )
| A. |  | |
| B. | 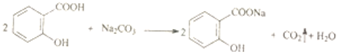 | |
| C. | 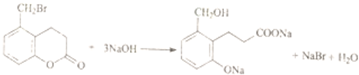 | |
| D. | 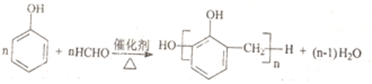 |
3.下列反应中,属于取代反应的是( )
| A. | 将苯滴入溴水中,振荡后水层接近无色 | |
| B. | 乙烯使酸性KMnO4溶液褪色 | |
| C. | 甲烷与氯气混合,光照后黄绿色变浅 | |
| D. | 乙烯使溴的四氯化碳溶液褪色 |
10.现有4摩尔铝及足量稀HCl和稀NaOH溶液,欲将铝全部转化为Al(OH)3,所需HCl与NaOH的物质的量之和最少应是( )
| A. | 6摩尔 | B. | 4摩尔 | C. | 16摩尔 | D. | 8摩尔 |
7.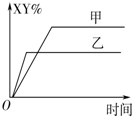 在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )
在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )
 在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )
在密闭容器中,反应X2(g)+Y2(g)?2XY(g)△H<0达到甲平衡,仅改变某一条件后,达到乙平衡.对此过程的分析正确的是( )| A. | 可能是减小了反应物的浓度,反应物X2转化率一定减小 | |
| B. | 可能是加入了催化剂,反应物X2百分含量(X2%)将增大 | |
| C. | 可能是缩小了容器的体积,但该反应的平衡常数保持不变 | |
| D. | 可能是升高了温度,该反应的平衡常数一定减小 |
8.下列说法中正确的是( )
| A. | 由Fe、Cu、FeCl3溶液组成的原电池中,负极反应式为:Cu-2e-═Cu2+ | |
| B. | 由Al、Mg、NaOH 溶液组成的原电池中,负极反应式为:Al+4OH--3e-═AlO2-+2H2O | |
| C. | 由Al、Cu、稀硫酸溶液组成的原电池中,负极反应式为:Cu-2e-═Cu2+ | |
| D. | 由Al、Cu、浓硝酸溶液组成的原电池中,负极反应式为:Al-3e-═Al3+ |