题目内容
【题目】常温下,将HC1气体通入到1L浓度均为0.1mol/L的NaA和NaB的混合溶液中,混合溶液的pH与离子浓度变化的关系如图所示(忽略溶液体积的变化)。下列叙述不正确的是
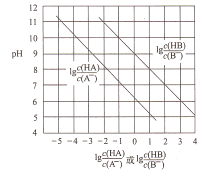
A. Ka(HB)的数量级为10-9
B. 酸性的强弱顺序为HCl>HA>HB
C. 当通入0.1molHC1气体时,c(B-)>c(A-)
D. 当混合溶液呈中性时,c(Na+)=c(Cl-)+c(A-)+c(B-)
【答案】C
【解析】A、根据图像可知,当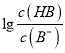 =3时,pH=6,此时,c(H+)=10-6mol/L,
=3时,pH=6,此时,c(H+)=10-6mol/L, 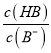 =103,Ka(HB)=
=103,Ka(HB)= 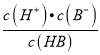 = 10-6×10-3=10-9,故A正确;B、pH一定时,
= 10-6×10-3=10-9,故A正确;B、pH一定时, 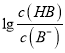 >
>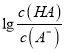 ,则有
,则有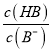 >
>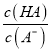 ,
, 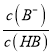 <
<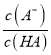 ,式子两边都乘以c(H+),可得
,式子两边都乘以c(H+),可得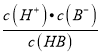 <
<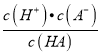 ,即Ka(HB)<Ka(HA),所以酸性HA>HB,向NaA和NaB的混合溶液中通入HCl后,溶液中存在HA、HB,则说明HCl酸性强于HA和HB,所以酸性强弱顺序为HCl>HA>HB,故B正确;C、原溶液中NaA和NaB均为0.1mol,根据强酸制弱酸原理,通入0.1molHCl,H+先与B-反应,反应后溶液中溶质为0.1molNaA、0.1molNaCl、0.1molHB,NaA完全电离,微弱水解,而HB部分电离,所以溶液中c(B-<c(A-),故C错误;D、混合溶液的电荷守恒为:c(Na+)+c(H+)=c(Cl-)+c(A-)+c(B-)+c(OH-),当溶液呈中性时,c(H+)= c(OH-),所以有c(Na+)+c(H+)=c(Cl-)+c(A-)+c(B-)+c(OH-),故D正确。故选C。
,即Ka(HB)<Ka(HA),所以酸性HA>HB,向NaA和NaB的混合溶液中通入HCl后,溶液中存在HA、HB,则说明HCl酸性强于HA和HB,所以酸性强弱顺序为HCl>HA>HB,故B正确;C、原溶液中NaA和NaB均为0.1mol,根据强酸制弱酸原理,通入0.1molHCl,H+先与B-反应,反应后溶液中溶质为0.1molNaA、0.1molNaCl、0.1molHB,NaA完全电离,微弱水解,而HB部分电离,所以溶液中c(B-<c(A-),故C错误;D、混合溶液的电荷守恒为:c(Na+)+c(H+)=c(Cl-)+c(A-)+c(B-)+c(OH-),当溶液呈中性时,c(H+)= c(OH-),所以有c(Na+)+c(H+)=c(Cl-)+c(A-)+c(B-)+c(OH-),故D正确。故选C。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是_____,最活泼的非金属元素是_______________
(2)化学性质最不活泼的元素是______________,其原子的原子结构示意图为___________;
(3)元素的最高价氧化物对应的水化物中酸性最强的是______________,碱性最强的是____________,
(4)在③~⑦元素中,原子半径最大的是________,原子半径最小的是_______;
【题目】下表是元素周期表的前三周期:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0[ | |
一 | A | |||||||
二 | B | C | D | E | F | |||
三[ | G | H | I | J |
回答下列问题:
(1)J元素的元素的名称:___________。
(2)G元素与I 元素形成的化合物的电子式是___________,
A、G、E形成的化合物中含有的化学键类型为_____________________________。
(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是_____________,
属于两性氢氧化物的是_______________(用化合物的化学式表示)。
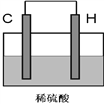
(4)将H单质与C的一种单质(导体)按如下图装置连接,其中C极为_________极(填正或负),并写出该电极反应式为:____________________。