题目内容
【题目】已知p(A)=-lgc(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
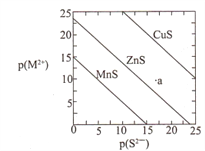
A. a点无ZnS沉淀生成
B. 可用MnS除去MnCl2溶液中混有的少量ZnCl2
C. 向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)增大
D. CuS和MnS共存的悬独液中,![]()
【答案】C
【解析】p(A)=-lgc(A),则c(A)=10-p(A)mol/L,故p(A)越大,c(A)越小 。所以平衡曲线右上方为不饱和溶液,平衡曲线左下方为过饱和溶液。A、a点不饱和,没有ZnS沉淀析出,故A正确;B、MnS的溶解度大于ZnS,向MnCl2溶液中加入MnS固体,可以促使平衡MnS(s)+Zn2+ ZnS(s)+Mn2+向右移动,即MnS转化为更难溶的ZnS,达到除去Zn2+的目的,故B正确;C、
向CuS悬浊液中加入少量水,平衡向溶解的方向移动,由于悬浊液中存在CuS固体,溶液依然是饱和的,所以c(S2-)不变,故C错误;D、当p(S2-)=0,p(Mn2+)=15,即c(S2-)=1mol/L时,c(Mn2+)=10-15mol/L,Ksp(MnS)= c(Mn2+)×c(S2-)=10-15;当p(S2-)=25,p(Zn2+)=25,即c(S2-)=10-25mol/L,c(Zn2+)=10-10mol/L,Ksp(ZnS)= c(Zn2+)×c(S2-)=10-35;CuS和MnS共存的悬独液中, ![]() =10-20,故D正确。故选C。
=10-20,故D正确。故选C。

【题目】现有一瓶甲和乙的混合物,已知甲和乙的某些性质如表所示,据此将甲和乙互相分离的方法是( )
物质 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | 水中溶解性 |
甲 | -98 | 57.5 | 0.93 | 可溶 |
乙 | -84 | 87 | 0.90 | 可溶 |
A. 蒸馏法 B. 结晶法 C. 萃取法 D. 过滤法