题目内容
13.短周期元素X、Y、Z在周期表中的相对位置如图所示,则下列说法正确的是( )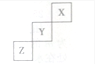
| A. | Z的最高价氧化物的水化物是强酸 | |
| B. | Y是气态氢化物稳定性小于Z的气态氢化物 | |
| C. | Z一定是活泼的金属 | |
| D. | 1molZ单质在足量的氧气中燃烧时,有6mol电子发生转移 |
分析 三种元素在短周期中的不同周期,则X一定位于第一周期,且在周期表的右侧,则一定为He,根据其它两种元素的相对位置可知Y为F元素,Z为S元素,根据元素所在位置结合元素周期律的递变规律比较单质、含氧酸的性质.
解答 解:三种元素在短周期中的不同周期,则X一定位于第一周期,且在周期表的右侧,则一定为He,根据其它两种元素的相对位置可知Y为F元素,Z为S元素,
A、Z为S元素,Z的最高价氧化物的水化物是H2SO4,H2SO4为强酸,故A正确;
B、Y为F元素,Z为S元素,非金属性F>S,氟化氢的稳定性强于硫化氢,故B错误;
C、X为He,Y为F,Z为S,三种元素都是非金属元素,故C错误;
D、Z为S元素,1molZ单质在足量的氧气中燃烧时,有4mol电子发生转移,故D错误;
故选A.
点评 本题考查元素的位置、性质的相互关系及应用,题目难度不大,注意元素周期表中元素性质的递变性和相似性.

练习册系列答案
相关题目
1.将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:A(g)+B(g)?C(g)+D(g),并达到平衡.C的体积分数随时间变化如图Ⅰ中曲线b所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )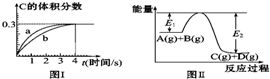

| A. | 该温度下,反应的平衡常数数值约为7.36 | |
| B. | 恒温条件下,缩小反应容器体积可以使反应的过程按图Ⅰ中a曲线进行 | |
| C. | 反应在第4秒钟达到化学平衡状态,0~4秒内,以A表示的化学反应速率是:0.225 mol•L-1•s-1 | |
| D. | 在上述反应体系中加入催化剂,化学反应速率增大,E1和E2均减小 |
18.煤化工是以煤 为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工 产品的工业过程.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,△S=+133.7J•(K•mol)-1
①该反应能否自发进行与温度 有关;
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是bc(填字母).
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2molH-O键
c.v正(CO)=v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
①实验1中以v(CO2) 表示的反应速率为0.16mol•(L•min)-1.
②该反应的逆反应为吸热(填“吸”或“放”)热反应
③该反应平衡常数的数学表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$表中x=$\frac{4}{3}$; y=$\frac{8}{3}$.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,△S=+133.7J•(K•mol)-1
①该反应能否自发进行与温度 有关;
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是bc(填字母).
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2molH-O键
c.v正(CO)=v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 3 | 0.75 | 2.25 | 3 |
| 3 | 900 | 2 | 4 | x | y | t |
②该反应的逆反应为吸热(填“吸”或“放”)热反应
③该反应平衡常数的数学表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$表中x=$\frac{4}{3}$; y=$\frac{8}{3}$.
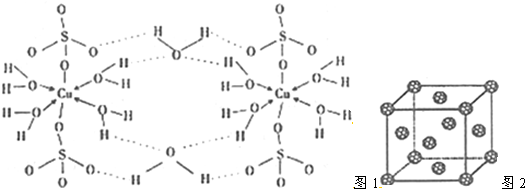
5.(1)胆矾CuSO4•5H2O的结构示意图1如下,其含有的微粒间作用力有abde(填序号)
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
(2)根据等电子原理,写出与CO2等电子体的分子和离子各一种N2O或CS2、CNO-或SCN-或NO2+;1molO22+中含有的π键数目为2NA
(3)已知
分析表中四种物质的相关数据,请回答
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是C-H键的键能大于Si-H键的键能,N-H键的键能大于P-H键的键能,因此分解温度CH4的分解温度高于SiH4,NH3的分解温度高于PH3
(4)C60形成晶体的晶胞结构如图2所示,则每个C60分子周围距离最近的C60分子由12个,若晶胞参数为pnm,列出计算该晶体的密度$\frac{4×720}{(p×1{0}^{-7})^{3}{N}_{A}}$g•cm-3(阿伏伽德罗常数用NA表示)
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
(2)根据等电子原理,写出与CO2等电子体的分子和离子各一种N2O或CS2、CNO-或SCN-或NO2+;1molO22+中含有的π键数目为2NA
(3)已知
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是C-H键的键能大于Si-H键的键能,N-H键的键能大于P-H键的键能,因此分解温度CH4的分解温度高于SiH4,NH3的分解温度高于PH3
(4)C60形成晶体的晶胞结构如图2所示,则每个C60分子周围距离最近的C60分子由12个,若晶胞参数为pnm,列出计算该晶体的密度$\frac{4×720}{(p×1{0}^{-7})^{3}{N}_{A}}$g•cm-3(阿伏伽德罗常数用NA表示)

 后静置,放出水层(废液).
后静置,放出水层(废液).