题目内容
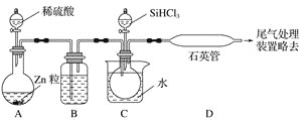
【题目】氮化铝(AlN)是一种灰白色固体,能与水缓慢反应。利用NH3和Al在800℃以上反应可制备AlN,实验装置如下:
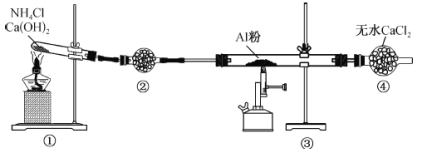
回答下列问题:
(1)装置②中盛放的药品为__________;装置④的作用是吸收氨气和__________。
(2)实验时先点燃①处酒精灯,其目的是______________________________________。
(3)为使实验安全,装置④的尾气处理方法是_____________________。
(4)装置①中发生反应的化学方程式为_____________________;装置③中发生反应的化学方程式为____________________。
【答案】碱石灰(或生石灰或氢氧化钠固体) 防止空气中水蒸气的进入 排尽装置内的空气 气体通到室外或烧掉 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 2Al+2NH3
MnCl2+Cl2↑+2H2O 2Al+2NH3![]() 2AlN+3H2
2AlN+3H2
【解析】
(1)装置②中盛放的药品应为能吸收NH3中的水蒸气,但与NH3不反应的固体;
装置④的作用是吸收氨气和防止空气中某成分的进入,从而导致AlN的变质。
(2)因为反应产生H2,H2与空气混合加热,易发生爆炸,所以实验时先点燃①处酒精灯,以便排尽装置内的空气。
(3)装置④的尾气中混有H2,它易燃易爆,为使实验安全,应进行处理。
(4)装置①中发生反应为实验室制氨气的反应;装置③中发生反应为铝与氨气的置换反应。
(1)装置②中盛放的药品应为能干燥NH3的固体,即为碱石灰(或生石灰或氢氧化钠);
装置④的作用是吸收氨气和防止空气中水蒸气的进入。答案为:碱石灰(或生石灰或氢氧化钠);防止空气中水蒸气的进入;
(2)实验时先点燃①处酒精灯,其目的是产生气体将装置内的空气排出,防止生成的H2与空气混合发生爆炸。答案为:排尽装置内的空气;
(3)为使实验安全,装置④的尾气处理方法是将气体通到室外或烧掉。答案为:气体通到室外或烧掉;
(4)装置①中发生反应为实验室制氨气的反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;装置③中发生反应为铝与氨气的置换反应2Al+2NH3
MnCl2+Cl2↑+2H2O;装置③中发生反应为铝与氨气的置换反应2Al+2NH3![]() 2AlN+3H2。答案为:MnO2+4HCl(浓)
2AlN+3H2。答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;2Al+2NH3
MnCl2+Cl2↑+2H2O;2Al+2NH3![]() 2AlN+3H2。
2AlN+3H2。