题目内容
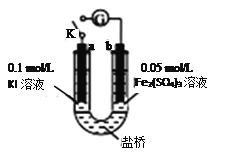
【题目】根据氧化还原反应Zn+2H+=Zn2++H2↑设计一个原电池?并判断正负极、写出各电极电极反应方程和反应的类型(在方框内画出原电池装置图) 负极:
正极:
负极反应:
正极反应:
负极反应类型:
正极反应类型:
原电池装置图: .
【答案】锌;铜;Zn﹣2e﹣═Zn2+;2H++2e﹣═H2↑;氧化反应;还原反应;
【解析】解:该原电池中,负极材料为金属锌,正极材料可以为铜棒或活泼性比锌若的其它金属材料,电解质溶液为稀硫酸或者稀盐酸,据此画出该原电池装置图为:  ,负极是锌,正极是铜,负极发生氧化反应,电极反应式为:Zn﹣2e﹣═Zn2+;氢离子在正极得到电子生成氢气,发生得到电子,发生还原反应,电极反应为:2H++2e﹣═H2↑,所以答案是:锌;铜;Zn﹣2e﹣═Zn2+;2H++2e﹣═H2↑;氧化反应;还原反应;
,负极是锌,正极是铜,负极发生氧化反应,电极反应式为:Zn﹣2e﹣═Zn2+;氢离子在正极得到电子生成氢气,发生得到电子,发生还原反应,电极反应为:2H++2e﹣═H2↑,所以答案是:锌;铜;Zn﹣2e﹣═Zn2+;2H++2e﹣═H2↑;氧化反应;还原反应;  .
.

 名校课堂系列答案
名校课堂系列答案【题目】在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g)![]() 2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强 | P1 | P2 | P3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A. 2 c1>c3 B. a + b=92.4 C. 2P1<P3 D. α1 +α3=1
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)![]() MgO(s)+SO2(g)+ CO2(g) ΔH>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s)+SO2(g)+ CO2(g) ΔH>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
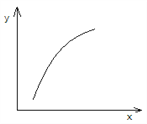
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |