题目内容
卤素单质的性质与F2>Cl2>Br2>I2的变化规律不相符的是( )
| A、与氢气反应的剧烈程度 |
| B、气态氢化物的稳定性 |
| C、单质还原性的强弱 |
| D、与水反应的剧烈程度 |
考点:卤素原子结构及其性质的比较
专题:元素周期律与元素周期表专题
分析:元素原子结构的变化决定其性质的变化.同一主族元素随着元素原子核电荷数的递增,原子半径、离子半径逐渐增大,原子核与最外层电子之间的距离增大,原子核对最外层电子的引力减弱,得电子能力减弱,单质的氧化性减弱;因为非金属性逐渐减弱,形成的氢化物稳定性也逐渐减弱,以此解答该题.
解答:
解:A.非金属性F>Cl>Br>I,则与氢气反应的难易程度为由易到难,与上述规律一致,故A不选;
B.非金属性F>Cl>Br>I,则对应的氢化物稳定性为由强到弱,与上述规律一致,故B不选;
C.非金属性F>Cl>Br>I,单质的还原性逐渐增强,与上述规律不一致,故C选;
D.非金属性F>Cl>Br>I,单质的活泼性F2>Cl2>Br2>I2,水与反应的剧烈程度逐渐减弱,与上述规律一致,故D不选.
故选C.
B.非金属性F>Cl>Br>I,则对应的氢化物稳定性为由强到弱,与上述规律一致,故B不选;
C.非金属性F>Cl>Br>I,单质的还原性逐渐增强,与上述规律不一致,故C选;
D.非金属性F>Cl>Br>I,单质的活泼性F2>Cl2>Br2>I2,水与反应的剧烈程度逐渐减弱,与上述规律一致,故D不选.
故选C.
点评:本题考查非金属性的比较,为高频考点,把握元素的位置及元素周期律为解答的关键,注意非金属性比较方法及应用,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列分子或离子在相应条件下能大量共存的是( )
| A、常温常压下混合气体:C2H4、CO2、NO、O2 |
| B、澄清透明的溶液中:Na+、K+、MnO4-、ClO- |
| C、室温下,c(H+)=1.0 mol/L的溶液中:K+、Fe3+、SO42-、C6H5O- |
| D、能溶解Al(OH)3的溶液:NH4+、K+、C1-、CO32- |
 如图为元素周期表中短周期的一部分,其中b原子的最外层电子数为电子层数的两倍,则下列叙述中正确的是( )
如图为元素周期表中短周期的一部分,其中b原子的最外层电子数为电子层数的两倍,则下列叙述中正确的是( )| A、b的元素符号为C |
| B、a元素的最高正化合价为+6 |
| C、c元素的最高正化合价为+5 |
| D、b元素的气态氢化物的化学式为H2S |
25℃时,弱酸的电离平衡常数如表:
下列有关说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
| A、等物质的量浓度的各溶液的pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B、a mol/L HCN与a mol/L NaOH溶液等体积混合后所得溶液呈中性 |
| C、往冰醋酸中逐滴加水稀释,溶液导电能力始终保持减小 |
| D、在Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl═NaCl+N2↑+2H2O.关于该反应的下列说法,正确的是( )
| A、N2既是氧化剂,又是还原剂 |
| B、NH4Cl中的氮元素被还原 |
| C、被氧化的氮原子与被还原的氮原子之比为1:1 |
| D、每生成1mol N2时,转移电子的物质的量为6mol |
下面关于氢化物的叙述正确的是( )
| A、一个D2O分子所含的中子数为8 |
B、NH3的结构式为: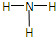 |
C、HCl的电子式为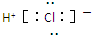 |
| D、热稳定性:HCl>HF |
已知:①CH3OH(g)+H2O(g)═CO2(g)+3H2(g),△H=+49.0kJ?mol-1;②CH3OH(g)+
O2(g)=CO2(g)+2H2(g),△H=-192.9kJ?mol-1.下列说法正确的是( )
| 1 |
| 2 |
A、根据②推知反应:CH3OH(l)+
| ||
| B、①反应中,反应物的总能量高于生成物总能量 | ||
| C、CH3OH转变成H2的过程一定要吸收能量 | ||
D、反应②中的能量变化如图所示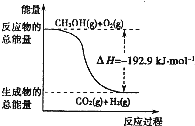 |