题目内容
【题目】NH3是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
共价键 | 键能/ kJ·mol-1 |
H―H | 436 |
N≡N | 946 |
N―H | 391 |
注:拆开气态物质中1 mol某种共价键需要吸收的能量,就是该共价键的键能。
N2 (g)+3 H2 (g)![]() 2 NH3 (g) H =____kJ·mol-1
2 NH3 (g) H =____kJ·mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2 +3H2 ![]() 2NH3,测得各组分浓度随时间变化如图1所示。
2NH3,测得各组分浓度随时间变化如图1所示。
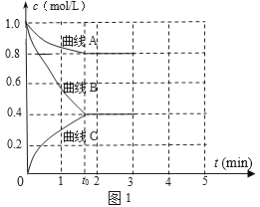
①表示c(N2)的曲线是__(填“曲线A”、“曲线B”或“曲线C”)。
②0~t0时用H2表示反应速率v(H2)____mol·L-1·min-1。
③下列能说明该反应达到平衡的是____。
a.混合气体的压强不再变化
b.2c(H2)= 3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:
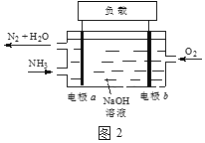
①电极b名称是____。
②电解质溶液中OH-离子向____移动(填“电极a”或“电极b”)。
③电极a的电极反应式为____。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是____。
【答案】 -92 曲线A 0.6/t0 a d 正极 电极a 2NH3 + 6OH--6e- = N2 + 6H2O 2NH3 + NaClO = N2H4+ NaCl + H2O
【解析】(1)反应热的焓变△H=反应物总键能-生成物总键能,N2 (g)+3 H2 (g)![]() 2 NH3 (g) H =436×3+946×1-391×6=-92kJ·mol-1,故答案为:-92;
2 NH3 (g) H =436×3+946×1-391×6=-92kJ·mol-1,故答案为:-92;
(2)①在恒容的密闭容器中充入N2和H2发生反应:N2 +3H2 ![]() 2NH3,随着反应的进行,氮气的浓度逐渐减小,减小幅度比氢气小,因此表示c(N2)的曲线是曲线A,故答案为:曲线A;
2NH3,随着反应的进行,氮气的浓度逐渐减小,减小幅度比氢气小,因此表示c(N2)的曲线是曲线A,故答案为:曲线A;
②0~t0时用H2表示反应速率v(H2)=![]() =
= ![]() mol·L-1·min-1,故答案为:
mol·L-1·min-1,故答案为:![]() ;
;
③a.恒容的密闭容器,压强逐渐减小,混合气体的压强不再变化,能说明达到平衡,正确;b.2c(H2)= 3c(NH3)不能说明浓度是否变化,因此不能说明达到平衡,错误;c.根据质量守恒定律,混合气体的质量始终不变,不能说明达到平衡,错误;d.NH3的体积分数不再变化,说明正逆反应速率相等,能说明达到平衡,正确;故选ad;
(3)①在燃料电池中通入燃料的为负极,氧气的为正极,则电极a为负极,电极b为正极,故答案为:正极;
②在燃料电池中电解质溶液中OH-离子向电极a移动,故答案为:电极a;
③在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极a为负极,发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O故答案为:2NH3+6OH--6e-═N2+6H2O。
(4)NH3与NaClO反应来制得火箭燃料肼(N2H4),反应的化学反应方程式为2NH3 + NaClO = N2H4+ NaCl + H2O,故答案为:2NH3 + NaClO = N2H4+ NaCl + H2O。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案【题目】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
A | ||||||||
B | C | |||||||
D | E | F | ||||||
回答下列问题:
(1)元素B的元素符号为______,它在元素周期表中的位置是__________。
(2)D的简单离子的结构示意图为_________,它的最高价氧化物对应水化物中含有的化学键有_____________,D单质与水反应的化学方程式为____________________。
(3)用电子式表示EF2的形成过程_________________________________。
(4)由A2、C2构成碱性燃料电池,则该电池的负极反应方程式为_______________,该电池工作过程中每通过2mol电子所需要的C2体积为___________(标准状况)。
(5)C和D在高温条件下形成化合物的化学式为_________,与二氧化碳反应的化学方程式为_________________________。
