题目内容
14.下列叙述错误的是( )| A. | 在热化学方程式中,物质化学式前面的化学计量数可以为整数也可以为简单分数 | |
| B. | 同一化学反应,热化学方程式中物质的化学计量数不同,反应的△H也不同 | |
| C. | 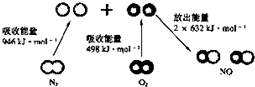 N2(g)与O2(g)反应生成NO(g)过程中的能量变化如图所示,若加入催化剂,化学反应速率改变,△H也改变 N2(g)与O2(g)反应生成NO(g)过程中的能量变化如图所示,若加入催化剂,化学反应速率改变,△H也改变 | |
| D. | 化学反应中化学键的断裂和形成是反应过程中有能量变化的本质原因 |
分析 A、在热化学方程式中,物质化学式前面的化学计量数只表示物质的量;
B、反应热与物质的化学计量数成正比;
C、若加入催化剂,化学反应速率改变,但反应物和生成物的总能量不变,所以△H不改变;
D、根据化学反应中实质是化学键的断裂和形成.
解答 解:A、在热化学方程式中,物质化学式前面的化学计量数只表示物质的量,所以物质化学式前面的化学计量数可以为整数也可以为简单分数,故A正确;
B、反应热与物质的化学计量数成正比,所以热化学方程式中物质的化学计量数不同,反应的△H也不同,故B正确;
C、若加入催化剂,化学反应速率改变,但反应物和生成物的总能量不变,所以△H不改变,故C错误;
D、因化学反应中能量变化的主要原因是化学键的断裂和形成,故D正确;
故选C.
点评 本题主要考查了化学反应中能量变化的原因,难度不大,需要强调的是反应是吸热反应还是放热反应与反应的条件无关.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
9.高温条件下反应达到平衡时的平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容条件下升高温度,H2浓度减小.则下列说法正确的是( )
| A. | 反应的热化学方程式可表示为:CO(g)+H2O(g)$?_{高温高压}^{催化剂}$CO2(g)+H2(g)△H<0 kJ/mol | |
| B. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应的正反应为放热反应 |
19.维生素C(化学式为C6H8O6)是一种重要的维生素,它能促进人体生长发育,增强人体对疾病的抵抗力.下列有关说法不正确的是( )
| A. | 维生素C属于水溶性维生素 | B. | 维生素C是一种较强的还原剂 | ||
| C. | 维生素C水溶液显碱性,味道可口 | D. | 维生素C主要存在于蔬菜和水果中 |
6.若将pH=2的酸溶液和pH=12的NaOH溶液等体积混和.混和液中的pH值为( )
| A. | 等于7 | B. | 大于等于7 | C. | 小于等于7 | D. | 无法判断 |
4.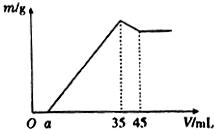 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )
 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )| A. | 3.50mol/L | B. | 1.75mol/L | C. | 0.85mol/L | D. | 无法计算 |
 金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示:
金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示: