题目内容
【题目】甲酸乙酯为允许使用的食用香料,又称蚁酸乙酯,有辛辣的刺激味和菠萝样的果香香气,还有强烈朗姆酒似香气,并略带苦味。
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点如下
试剂 | 乙醚 | 乙醇 | 甲酸 | 甲酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 100.5 | 54.4 |
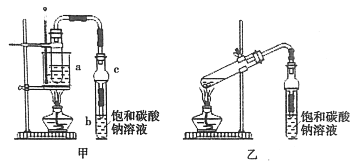
(1)制备粗品
将4mL乙醇、3mL甲酸和2mL浓硫酸加入试管a中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管b内得到甲酸乙酯的粗品。
①实验时,加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是__________;浓硫酸用量又不能过多,原因是_________。
②球形干燥管C的作用是__________。
③若用乙装置制备甲酸乙酯,其缺点有__________。
(2)制备精品
①反应结束后,从试管b中分离出甲酸乙酯粗品所用的主要仪器__________。
②从b中分离出的甲酸乙酯中常含有少量的乙醇、乙醚和水,应先加入无水氯化钙,除去______,然后再通过_________操作得到甲酸乙酯。
③某同学用装有饱和氢氧化钠的试管收集甲酸乙酯,几乎没有收集到产物。原因是______________(用化学方程式解释)。
【答案】 浓H2SO4能吸收生成的水,使平衡向生成酯的方向移动,提高酯的产率 浓H2SO4具有强氧化性和脱水性,会使有机物碳化,降低酯的产率 防止倒吸、冷凝 受热不均匀,不易于控制温度;原料损失较大、易发生副反应 分液漏斗 乙醇和水 蒸馏 HCOOCH2CH3+NaOH →HCOONa+CH3CH2OH
【解析】(1)①酯化反应过程中浓硫酸的作用是催化剂和吸水剂,利用适量浓H2SO4能吸收生成的水,使平衡向生成酯的方向移动,提高酯的产率;但浓硫酸有强氧化性和脱水性,多余的浓硫酸能使有机物碳化或氧化,降低原料利用率降低,导致产率降低;
②利用球形干燥管C可以防止倒吸和产物冷凝;
③若用乙装置制备甲酸乙酯,因温度不易控制,且加热面积小,导致反应混合物受热不均匀,原料损失较大、易发生副反应;
(2)①酯不易溶于水溶液,反应混合物静止后会分层,可利用分液漏斗进行分液操作分离;
②甲酸乙酯中常含有少量的乙醇、乙醚和水,可利用无水氯化钙吸水,再利用沸点差异,通过蒸馏操作得到甲酸乙酯;
③因酯在碱性条件下易水解,发生反应HCOOCH2CH3+NaOH →HCOONa+CH3CH2OH,故用装有饱和氢氧化钠的试管收集甲酸乙酯,几乎没有收集到产物。

 名校课堂系列答案
名校课堂系列答案