题目内容
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A. 20gD2O与20g氖气所含有的电子数相同
B. 标准状况下,22.4L二氯甲烷的分子数约为NA
C. 常温常压下,100g 17%的双氧水溶液中含有氧原子总数为NA
D. 56g铁与一定量的氯气在一定条件下充分反应,转移的电子数一定为3NA
【答案】A
【解析】A.D2O的相对分子质量为20,根据n=![]() 结合原子的组成分析判断;B.标准状况下,二氯甲烷的状态不是气体;C、过氧化氢水溶液中水分子中也含氧原子;D.铁与氯气反应生成氯化铁,依据完全反应的物质结合方程式计算转移的电子数。
结合原子的组成分析判断;B.标准状况下,二氯甲烷的状态不是气体;C、过氧化氢水溶液中水分子中也含氧原子;D.铁与氯气反应生成氯化铁,依据完全反应的物质结合方程式计算转移的电子数。
A.20gD2O的物质的量=![]() =1mol,含有电子10mol,20g氖气的物质的量=
=1mol,含有电子10mol,20g氖气的物质的量=![]() =1mol,含有的电子为10mol,所含有的电子数相同,故A正确;B.标况下二氯甲烷不是气体,不能使用标况下的气体摩尔体积计算二氯甲烷的物质的量,故B错误;C、100 g 17% H2O2水溶液中过氧化氢物质的量为=
=1mol,含有的电子为10mol,所含有的电子数相同,故A正确;B.标况下二氯甲烷不是气体,不能使用标况下的气体摩尔体积计算二氯甲烷的物质的量,故B错误;C、100 g 17% H2O2水溶液中过氧化氢物质的量为=![]() =0.5mol,溶剂水中也含有氧原子,100g 17% H2O2水溶液含氧原子总数大于NA,故C错误;D.56g铁与一定量的氯气在一定条件下充分反应,如果氯气足量转移的电子数一定是3NA,如果氯气不足,则铁剩余,转移电子数少于3NA,故D错误;故选A。
=0.5mol,溶剂水中也含有氧原子,100g 17% H2O2水溶液含氧原子总数大于NA,故C错误;D.56g铁与一定量的氯气在一定条件下充分反应,如果氯气足量转移的电子数一定是3NA,如果氯气不足,则铁剩余,转移电子数少于3NA,故D错误;故选A。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】下列说法正确的是( )
①增大浓度,或加热或加压,或使用催化剂,一定可以加快反应速率.
②气态氢化物的稳定性:H2O>NH3>SiH4
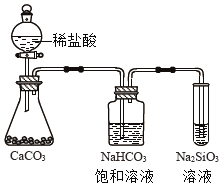
③如图所示实验可证明元素的非金属性:Cl>C>Si
|
④用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
A. ①②B. ②③C. ③④D. ②④
【题目】根据表中提供的部分短周期元素原子半径及主要化合价的信息,回答下列问题
元素代号 | A | B | C | D | E | F | G |
原子半径/nm | 0.186 | 0.160 | 0.143 | 0.112 | 0.104 | 0.099 | 0.066 |
主要化合价 | +1 | +2 | +3 | +2 | +6、-2 | +7、-1 | -2 |
(1)A在元素周期表中位置是____。
(2)B的离子结构示意图:_____,
(3)C单质与A的最高价氧化物对应的水化物反应的离子方程式:____。
(4)元素最高价氧化物对应的水化物酸性最强的是:____ (写化学式)。
(5)A元素与F元素形成的化合物的电子式 _____。