题目内容
1.K2[Na(CN)4]的名称为四氰合镍(Ⅱ)酸钾,中心原子采取dsp2杂化,配离子的空间构型为平面正方形.分析 配合物中,配离子:含有配位键的离子,可以是阳离子或阴离子;内界、外界:内界指配位单元,外界与内界相对;
配位体:提供孤电子对的分子或离子;配位原子:配体中,提供电子对的原子;
配合物命名:配离子时,配位体的名称放在前,中心原子名称放在后;配位体和中心原子的名称之间用“合”字相连;中心原子为离子者,在金属离子的名称之后附加带圆括号的罗马数字,以表示离子的价态;配位数用中文数字在配位体名称之前;如果配合物中有多种配位体,则它们的排列次序为:阴离子配位体在前,中性分子配位体在后;无机配位体在前,有机配位体在后,不同配位体的名称之间还要用中圆点分开;
根据K2[Ni(CN)4]首先找出内界、外界,然后找出中心离子,配位体,据此写出K2[Ni(CN)4]的名称,根据中心原子Ni的核外电子排布以及配位数判断其杂化类型,根据杂化类型判断配离子的空间构型.
解答 解:K2[Ni(CN)4]中中心原子Ni,配位体为CN-,外界离子为K+,每个K++1价,每个CN-为-1价,根据呈电中性,Ni的化合价为+2价,所以K2[Ni(CN)4]的名称为:四氰合镍(Ⅱ)酸钾,
中心原子Ni外层电子排布为3d84s2,镍(Ⅱ)外层为3d8,3d轨道上8个电子,配位体为CN-,外界离子为K+,所以Ni2+是6配位,需要6个杂化轨道,K+外层没有电子,分别需两个电子和两个K+成键,CN-的C有一对孤对电子,6个杂化轨道需要4个电子,三个3d轨道上有4个电子,其余2个3d轨道全充满4个电子,未参与杂化,还有三个轨道即空的4s、两个4p轨道,所以Ni2+为d3sp2杂化,Ni2+位于正方形中心,4个CN-离子分别占据4个角顶,因此配离子的空间构型为平面正方形,
故答案为:四氰合镍(Ⅱ)酸钾;dsp2;平面正方形.
点评 本题考查由配合物名称以及配合物中心离子的杂化,注意把握配合物内界、外界、中心离子、配位体的判断,根据配位体和中心离子命名,配合物中心离子的杂化为该题的难点,题目难度中等.

| A. | Al2O3 | B. | NaAlO2 | C. | Mg(OH)2 | D. | NaHCO3 |
| 选项 | 酸溶液 | c(NaOH) |
| A | pH=1的硫酸 | 0.4mol/L |
| B | pH=1的硝酸 | 0.4mol/L |
| C | 0.1mol/L的硫酸 | 0.2mol/L |
| D | 0.1mol/L的盐酸 | 0.2mol/L |
| A. | A | B. | B | C. | C | D. | D |
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓H2SO4稀释 ④KClO3分解制O2 ⑤生石灰跟水反应生成熟石灰 ⑥CaCO3高温分解 ⑦CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO ⑧Ba(OH)2•8H2O与固体NH4Cl混合 ⑨C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2 ⑩Al与HCl反应.
| A. | ①②④⑥⑦⑧⑨ | B. | ②④⑥⑦⑧⑨ | C. | ①④⑥⑧ | D. | ①②④⑧⑨ |
| A. | 原子核都是由质子和中子构成 | |
| B. | 质子数相同的粒子其化学性质不一定相同 | |
| C. | 某种粒子最外层上有8个电子,则一定是稀有气体元素的原子 | |
| D. | 原子电子构型为ns2np6的为稀有气体元素 |
| A. | 若管道漏气遇氨会产生白烟 | B. | 该反应利用了氯气的强氧化性 | ||
| C. | 该反应属于复分解反应 | D. | 生成1 mol N2有6 mol电子转移 |
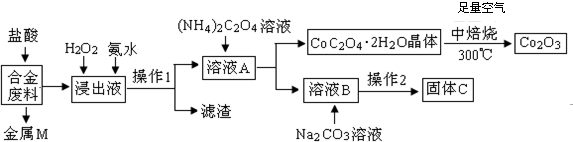
(1)金属M为Cu,操作1为过滤.
(2)加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O,加入氨水的作用是调节PH使Fe3+全部转化为氢氧化铁沉淀.
(3)由CoC2O4•2H2O转化为Co2 O3的化学方程式是4(CoC2O4?2H2O)+3O2$\frac{\underline{\;焙烧\;}}{\;}$2Co2O3+8H2O+8CO2.
(4)知Li2CO3微溶于水,且水溶液呈碱性.其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失,在常温条件下,饱和Li2CO3溶液中离子浓度由大到小的排列顺序为c(Li+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
 •
•