题目内容
某同学用0.10 mol/L的HCl溶液测定未知浓度的NaOH溶液,其实验操作如下:
A.用酸式滴定管量取20.00 mL HCl溶液注入锥形瓶,同时滴加2-3滴酚酞试液;
B.用0.10 mol/L的HC!溶液润洗酸式滴定管;
C.把滴定管用蒸馏水洗净;
D.取下碱式滴定管,用待测NaOH溶液润洗后,将待测NaOH溶液注入碱式滴定管至距离刻度“0”以上20 cm处,再把碱式滴定管固定好,调节液面;
E.检查滴定管是否漏水;
F.另取锥形瓶,再重复以上操作1-2次;
G.把锥形瓶放在碱式滴定管下边,瓶下垫一张白纸,边滴边摇动锥形瓶,直到加入最后一滴碱液后溶液颜色突变并在半分钟内不再变色为止,记下滴定管液面所在的刻度。
请回答下列问题:
(1)滴定操作的正确顺序是:(填字母) →C→ →B→ → → 。
(2)G步操作中在锥形瓶下垫一张白纸的作用是 。
(3)D步操作中液面应调节到 ,尖嘴部分应 。
(4)滴定终点读数时,如果仰视液面,读出的数值 ,若滴定前平视读数则由此计算得到的NaOH溶液浓度 (填“偏大”、“偏小”、“无影响”)
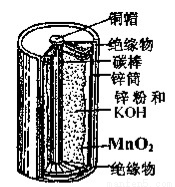
(5)如图分别是量筒、滴定管、温度计的一部分,则量筒,滴定管,温度计分别是 (填编号)。
(1)E C
C D
D B
B A
A G
G F (顺序填错一个不得分)
F (顺序填错一个不得分)
(2)便于观察锥形瓶内指示剂颜色的变化
(3)“0”刻度或“0”刻度以下; 充满溶液
(4)偏大 ;偏小
(5)②③①
【解析】
试题分析:(1)滴定管在使用之前需要查漏、洗涤和润洗,所以正确的的操作顺序是 E  C
C  D
D  B
B  A
A  G
G  F。
F。
(2)白纸可以便于观察溶液颜色的变化,有利于判断滴定终点。
(3)根据滴定管的构造可知,碱式滴定管中液面应调节到“0”刻度或“0”刻度以下,且尖嘴部分应充满溶液。
(4)滴定管的刻度自上而下是逐渐递增的,所以如果仰视液面,读出的数值偏大。所以导致消耗的氢氧化钠溶液体积增加,因此测定的浓度偏小。
(5)①是温度计,②是量筒(无0刻度且小刻度在下)③是滴定管,0刻度在上。
考点:考查中和滴定的操作、误差分析等

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案