题目内容
有甲、乙两位同学根据所学化学知识,设计了由铜和硫酸为原料制取硫酸铜的两种方案:①铜与浓硫酸直接反应,即Cu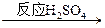 CuSO4。②由Cu
CuSO4。②由Cu CuSO4,试回答:
CuSO4,试回答:
(1)写出有关的化学反应方程式_______________、_______________、___________。(3分)
(2)这两种方案,你认为哪一种方案较合理?(1分)
(3)请说明选择合理方案的理由。(2分)
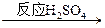 CuSO4。②由Cu
CuSO4。②由Cu CuSO4,试回答:
CuSO4,试回答:(1)写出有关的化学反应方程式_______________、_______________、___________。(3分)
(2)这两种方案,你认为哪一种方案较合理?(1分)
(3)请说明选择合理方案的理由。(2分)
(1)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O 2Cu+O2
CuSO4+SO2↑+2H2O 2Cu+O2 2CuO
2CuO
CuO+H2SO4====CuSO4+H2O
(2)方案②较合理。
(3)由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
 CuSO4+SO2↑+2H2O 2Cu+O2
CuSO4+SO2↑+2H2O 2Cu+O2 2CuO
2CuOCuO+H2SO4====CuSO4+H2O
(2)方案②较合理。
(3)由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
铜与浓硫酸直接反应方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,方案②先将铜变为CuO,方程式为2Cu+O2
CuSO4+SO2↑+2H2O,方案②先将铜变为CuO,方程式为2Cu+O2 2CuO,CuO再与硫酸作用生成CuSO4,方程式为CuO+H2SO4====CuSO4+H2O。(2)方案②较合理,因为由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
2CuO,CuO再与硫酸作用生成CuSO4,方程式为CuO+H2SO4====CuSO4+H2O。(2)方案②较合理,因为由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
 CuSO4+SO2↑+2H2O,方案②先将铜变为CuO,方程式为2Cu+O2
CuSO4+SO2↑+2H2O,方案②先将铜变为CuO,方程式为2Cu+O2 2CuO,CuO再与硫酸作用生成CuSO4,方程式为CuO+H2SO4====CuSO4+H2O。(2)方案②较合理,因为由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
2CuO,CuO再与硫酸作用生成CuSO4,方程式为CuO+H2SO4====CuSO4+H2O。(2)方案②较合理,因为由方程式可知,生成等质量的硫酸铜,所用Cu的质量相同,而耗硫酸的质量方案①是方案②的2倍,方案②节约原料;从环境保护角度看,方案①有SO2有毒气体生成,污染环境,而方案②不会造成环境污染。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
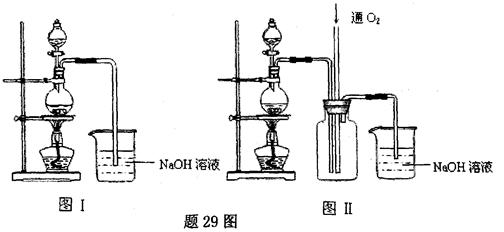
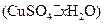 晶体中结晶水的含量时.测得有关数据如下表:
晶体中结晶水的含量时.测得有关数据如下表: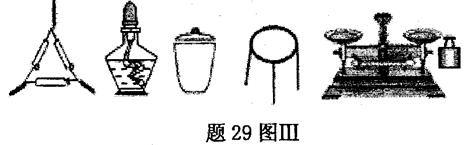
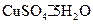 相比
相比 ) (填“偏高”、“偏低”、“不变”),可能的原因是 。(填字母序号)
) (填“偏高”、“偏低”、“不变”),可能的原因是 。(填字母序号)
 :MnCO3 115 MnO2 87 MnO 71)
:MnCO3 115 MnO2 87 MnO 71)