��Ŀ����
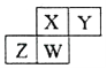
����Ŀ��������ͼ���ԴӲ�ͬ�Ƕ��о��������ʵ����ʼ���ת����ϵ��ͼ�мס���������Ԫ�ء��ش��������⣺
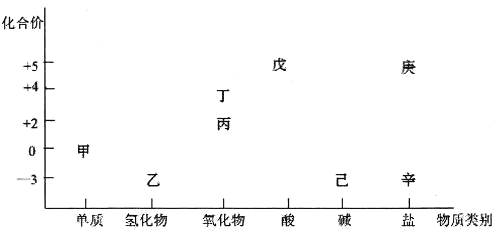
(1)���и�����ͼ������֮���ת������һ��ʵ�ֵ���__________��
A���ס��� B���ҡ��� C�������� D�������
(2)����˵����ȷ����____________��
A�����Ͷ���һ�������¶��������죬��������������
B�����ס��ҡ����������족���ǹ�ҵ�����ת������
C����������һ�������¶��������NaOH���������ң��������ҵ�ԭ����ͬ
D�����������Ϊͬ�����ʣ�������Һ��췴Ӧ�Ƶ�
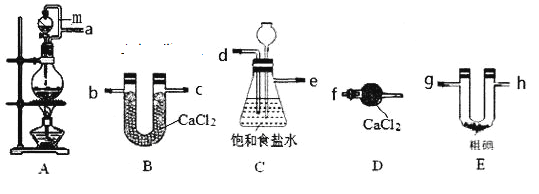
(3)�ȼҵ�����г����Ҽ�������ܵ��Ƿ�й©��������Ϊ______________________����֪��Ӧ�����л��м����ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ______________________________��
(4)��֪������������Һ��Ӧ���䷴Ӧ�Ļ�ѧ����ʽΪ��Fe+�����+��+��+H2O(����ʽδ��ƽ)���������б��Ͷ������ʵ���֮��Ϊ1��3��������������ʵ���֮��Ϊ_________�������������Ԫ�صļ�̬����ѡ�õ��Լ�Ϊ_________����Ӧ�����ӷ���ʽΪ___________��
���𰸡�CD BD �а������� 3Cl2+8NH3=N2+6NH4Cl 1��5 KSCN��Һ Fe3++3SCN-=Fe(SCN)3
��������
����NԪ�صĻ��ϼۼ���������������֪����N2������NH3������NO������NO2������HNO3������NH3H2O����Ϊ�����Ρ���Ϊ��Σ�Ȼ���������ʵ����ʷ������
����ͼʾ��NԪ�صĻ��ϼۼ�����������������֪����N2������NH3������NO������NO2������HNO3������NH3H2O����Ϊ�����Ρ���Ϊ��Ρ�
(1)A.������Ӧ��N2+O2 ![]() 2NO�����ܲ���NO2��A����
2NO�����ܲ���NO2��A����
B.4NH3+5O2![]() 4NO+6H2O�����ܲ���NO2��B����
4NO+6H2O�����ܲ���NO2��B����
C.3NO2+H2O=2HNO3+NO��C��ȷ��
D.3Cu��8HNO3(ϡ)=2Cu(NO3)2��2NO����4H2O��D��ȷ��
�ʺ���ѡ����CD��
(2)A.NO��NO2��һ�������¿��Է�����Ӧ����HNO3������Ӧ������NԪ�صĻ��ϼ۷����˱仯������NO��NO2���������������A����
B.�ڹ�ҵ�������ð��Ĵ�����������ȡ���ᣬ�����ķ�ӦΪ��N2+3H2 ![]() 2NH3��4NH3+5O2
2NH3��4NH3+5O2![]() 4NO+6H2O��2NO+O2=2NO2��3NO2+H2O=2HNO3+NO���ɼ��ڷ�Ӧ������ʵ���˼������������������ת����B��ȷ��
4NO+6H2O��2NO+O2=2NO2��3NO2+H2O=2HNO3+NO���ɼ��ڷ�Ӧ������ʵ���˼������������������ת����B��ȷ��
C.NH3H2O����Һ�д��ڵ���ƽ����NH3H2O![]() NH4++OH-��������Һ�м���NaOH����ʱ��c(OH-)����ƽ�������ƶ���NH3H2OŨ������NH3H2O�����ֽⷴӦ����������ͬʱNaOH�ܽ����Ҳ�ٽ���NH3H2O�ķֽ⣻�������NaOH�����ϼ��ȷ������Ǹ��ֽⷴӦ������������˶�����ȡ������ԭ����ͬ��C����
NH4++OH-��������Һ�м���NaOH����ʱ��c(OH-)����ƽ�������ƶ���NH3H2OŨ������NH3H2O�����ֽⷴӦ����������ͬʱNaOH�ܽ����Ҳ�ٽ���NH3H2O�ķֽ⣻�������NaOH�����ϼ��ȷ������Ǹ��ֽⷴӦ������������˶�����ȡ������ԭ����ͬ��C����
D.��Ϊ�����Σ���Ϊ��Σ�������Ϊͬһ�����ʣ����������NH4NO3������ͨ����ӦNH3+ HNO3=NH4NO3�õ���D��ȷ��
�ʺ���ѡ����BD��
(3)�ȼҵ�����г����Ҽ�������ܵ�������Ϊ������Ӧ��3Cl2+8NH3=N2+6NH4Cl��NH4Cl�ǰ�ɫ���壬����������ܵ�й©���ῴ���а��̲�����
(4)�������⼰��Ӧ������NO��NO2�����ʵ����ıȣ���ϵ����غ㡢ԭ���غ㣬�ɵ÷�Ӧ�Ļ�ѧ����ʽΪ��2Fe+10HNO3=2Fe(NO3)3+NO��+3NO2��+5H2O�����ݷ���ʽ��֪Fe��HNO3��Ӧ�����ʵ����ı�Ϊ1��5����Ӧ������Fe3+��������KSCN��Һ���顣����������Һ�еμӼ���KSCN��Һ����������Һ��ΪѪ��ɫ����֤������Fe3+����Ӧ�����ӷ���ʽΪFe3++3SCN-=Fe(SCN)3��