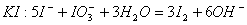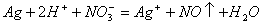题目内容
已知0.1 mol·L-1的二元酸H2A溶液的pH=4.0,则下列说法正确的是 ( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
【解析】0.1 mol·L-1的强酸pH=1.0,0.1 mol·L-1的H2A溶液pH=4.0,说明它是一种弱酸。Na2A发生水解A2-+H2O HA-+OH-和HA-+H2O
HA-+OH-和HA-+H2O H2A+OH-,溶液中存在HA-、A2-、H+、OH-;NaHA发生水解HA-+H2O
H2A+OH-,溶液中存在HA-、A2-、H+、OH-;NaHA发生水解HA-+H2O H2A+OH-和电离HA-
H2A+OH-和电离HA- H++A2-,溶液中存在HA-、A2-、H+、OH-,所以两溶液中离子种类相同,A不正确。
H++A2-,溶液中存在HA-、A2-、H+、OH-,所以两溶液中离子种类相同,A不正确。
物质的量相等的Na2A和NaHA因为存在上述水解、电离等过程,阴离子数量发生变化,所以阴离子总量不相等,B不正确。
由电荷守恒可知c(Na+)+c(H+)=c(HA-)+c(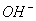 )+2c(A2-),C正确。Na2A溶液显碱性,c(
)+2c(A2-),C正确。Na2A溶液显碱性,c(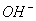 )>c(H+),D不正确
)>c(H+),D不正确
【答案】C

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
 (3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为 、另一种的晶胞如图二所示,该晶胞的空间利用率为 ,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为 、另一种的晶胞如图二所示,该晶胞的空间利用率为 ,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为  (保留两位有效数字)。(
(保留两位有效数字)。( )
)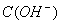 =1×2013—14mol·L-1,此溶液中一定可以大量共存的离子组是 ( )
=1×2013—14mol·L-1,此溶液中一定可以大量共存的离子组是 ( ) 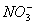 、
、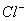 B. K+ 、Na+、
B. K+ 、Na+、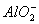 D. K+ 、 NH4+、
D. K+ 、 NH4+、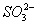 、
、 H++CH3COO-,下列叙述不正确的是 ( )
H++CH3COO-,下列叙述不正确的是 ( )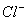 )>C(
)>C(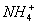 )>C(H+)>C(
)>C(H+)>C(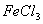 溶液与
溶液与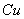 的反应:
的反应: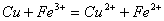
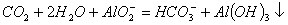
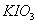 氧化酸性溶液中的
氧化酸性溶液中的