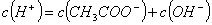题目内容
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是
A.将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多
B.盐酸和醋酸都可用相应的钠盐与浓硫酸反应制取
C.相同pH值的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH值变化大
D.相同pH值的盐酸和醋酸分别跟锌反应时,产生氢气的起始速度相等
【解析】A项中醋酸在稀释过程中电离程度加大,要想达到与盐酸一样的H+浓度,所需加水要多;B项中的醋酸不能用浓硫酸来制取;C项中HCl加NaCl不会使其电离有什么变化,因为它本来己经完全电离了,而醋酸中加醋酸钠,将会抑制醋酸的电离;D项中pH相同,c(H+)肯定相等,只能说明起始c(H+)相等,不能说明反应中有何变化。
【答案】AC。

练习册系列答案
相关题目
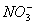 、Na+、
、Na+、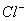 ,那么该溶液中还一定存在的离子是 ( )
,那么该溶液中还一定存在的离子是 ( ) 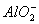 、
、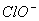 B.Mg2+、、
B.Mg2+、、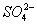 C.Fe2+ 、Cu2+ D.Ba2+、K+
C.Fe2+ 、Cu2+ D.Ba2+、K+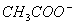 )>C(Na+)
)>C(Na+) 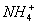 )+c(H+)=c(
)+c(H+)=c(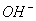 )+c(
)+c(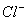 )
)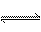 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
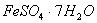 是常用的絮凝剂,它在水中最终生成__________沉淀(填化学式)。
是常用的絮凝剂,它在水中最终生成__________沉淀(填化学式)。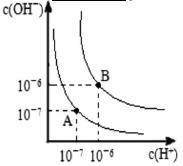
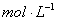 的NaOH溶液中,由水电离出的c(H+)=________
的NaOH溶液中,由水电离出的c(H+)=________