题目内容
某化学研究性学习小组探究Fe3+和SO32-之间发生的反应。
(1)取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。无气泡产生,无沉淀生成。这种红褐色液体是___________________。
(2)除了观察到以上的现象外,有成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为 。
研究性学习小组设计了两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
方案一:检验溶液中含有Fe2+证明发生了氧化还原反应
方案二:检验溶液中含有 证明发生了氧化还原反应
实验用品:0.1mol/L BaCl2、3mol/L盐酸、0.1mol/LKMnO4(H+)、氯水、20%KSCN、0.5mol/LKI;试管若干、胶头滴管若干
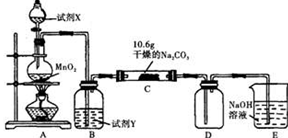
Ⅰ预处理:将(1)中获得的混合物放在如图装置中处理足够时间。

Ⅱ检验过程
(1)取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。无气泡产生,无沉淀生成。这种红褐色液体是___________________。
(2)除了观察到以上的现象外,有成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为 。
研究性学习小组设计了两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
方案一:检验溶液中含有Fe2+证明发生了氧化还原反应
方案二:检验溶液中含有 证明发生了氧化还原反应
实验用品:0.1mol/L BaCl2、3mol/L盐酸、0.1mol/LKMnO4(H+)、氯水、20%KSCN、0.5mol/LKI;试管若干、胶头滴管若干
Ⅰ预处理:将(1)中获得的混合物放在如图装置中处理足够时间。

Ⅱ检验过程
| 操 作 | 现象及结论 |
| 基于方案一: | |
| 基于方案二: | |
(1)Fe(OH)3胶体 (2)2Fe3++SO32-+H2O=2Fe2++SO42-+2H+ (3)SO42-
| 操作 | 现象及结论 |
| 基于方案一:取少量烧杯中的溶液于试管中,滴加20℅KSCN溶液,再加入适量氯水。 | 溶液开始不变色,加入氯水后变红色,证明溶液含有Fe2+ |
| 基于方案二:取少量烧杯中的溶液于试管中,加入足量3mol/L的盐酸,再滴加0.1mol/L BaCl2溶液。 | 溶液加盐酸时产生刺激性气体,当加入BaCl2有白色沉淀生成,证明含有SO42- |
试题分析:(1)FeCl3是强酸弱碱盐,水解使溶液显酸性; Na2SO3是强碱弱酸盐水解使溶液显碱性。当二者混合时,对彼此的水解起到了促进作用,所以产生了红褐色的氢氧化铁胶体。(2)如果二者混合发生氧化还原反应,则反应的两种方程式是:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+。在该反应中氧化剂Fe3+生成还原产物Fe2+;还原剂SO32-氧化为氧化产物SO42-。所以证明发生了氧化还原反应可以通过检验溶液中含有Fe2+或检验溶液中含有SO42-。方案一:利用Fe3+遇到SCN-产生血红色溶液,而Fe2+遇到SCN-不会发生反应,Fe2+遇到氯水被氧化为Fe3+后产生血红色溶液。来检验溶液中含有Fe2+。方案二:向溶液中加入足量3mol/L的盐酸使SO32-转化为SO2气体溢出,再滴加0.1mol/L BaCl2溶液,若产生白色沉淀,就证明含有SO42-。3+和SO32-之间发生的反应的原理。

练习册系列答案
相关题目