题目内容
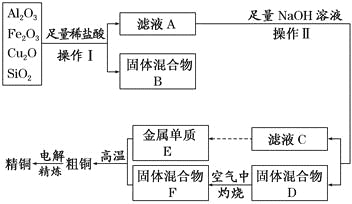
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
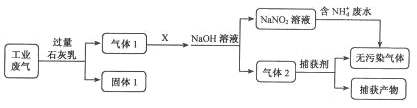
己知:NO+NO2+NaOH=NaNO2+H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
请回答下列问题:
(1)固体1中主要含有_________________________ (用化学式表示);
(2)X可以是________(填物质名称),且该物质需要________(填“少量”或“过量”);
(3)捕获剂所捕获的气体主要是________(用化学式表示);
(4)处理含NH4+废水时,发生反应的离子方程式为_________________________。
【答案】 Ca(OH)2、CaCO3、CaSO3 空气或氧气 少量 CO NH4++NO2-=N2↑+2H2O
【解析】工业废气中CO2、SO2可被石灰水吸收,生成CaCO3、CaSO3,气体不能被过量石灰水吸收的是N2、NO、CO,气体通入空气,用氢氧化钠溶液处理后到的NaNO2,通入空气但不能过量,否则得到硝酸钠,NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,则气体2含有CO、N2,经捕获剂得到氮气,防止污染空气,因此捕获剂所捕获的气体主要是CO。(1)工业废气中CO2、SO2可被石灰水吸收,生成CaCO3、CaSO3,因氢氧化钙过量,则废渣的成分为主要含有CaCO3、CaSO3、Ca(OH)2;(2)由分析可知,X是氧气或空气。过量空气会将NO氧化成NO3-,无法与NH4+发生反应,因此X不能过量;(3)根据以上分析可知,捕获剂所捕获的气体主要是CO;(4)NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,发生氧化还原反应,离子方程式为:NH4++NO2-=N2↑+2H2O。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案