题目内容
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.100 g46%的甲酸水溶液中所含的氧原子数目为 5NA
B.常温下,1L pH=7 的 lmolL-1 CH3COONH4 溶液中 CH3COO-与![]() 数目均为NA
数目均为NA
C.11 g由![]() H和
H和![]() O组成的超重水中,含有的中子数目为 5NA
O组成的超重水中,含有的中子数目为 5NA
D.高温下 ,5.6gFe 与足量的水蒸气反应,转移电子数为0.3NA
【答案】A
【解析】
A.100g46%的甲酸溶液中甲酸的质量为46g,物质的量为1mol,故含2NA个氧原子;而水的物质的量为54g,物质的量为3mol,故含3NA个氧原子,故溶液中共含5NA个氧原子,故A正确;
B.CH3COONH4 溶液中CH3COO-与![]() 均会发生水解,pH=7说明CH3COO-与
均会发生水解,pH=7说明CH3COO-与![]() 水解程度相同,但依然水解,所以该溶液中两种离子的数目均小于NA,故B错误;
水解程度相同,但依然水解,所以该溶液中两种离子的数目均小于NA,故B错误;
C.![]() H和
H和![]() O组成的超重水的摩尔质量为(3+3+16)g/mol =22g/mol,一个超重水分子中所含中子数为2+2+8=12,所以11g该超重水的物质的量为
O组成的超重水的摩尔质量为(3+3+16)g/mol =22g/mol,一个超重水分子中所含中子数为2+2+8=12,所以11g该超重水的物质的量为![]() =0.5mol,所含中子数为6NA,故C错误;
=0.5mol,所含中子数为6NA,故C错误;
D.5.6g铁物质的量为![]() =0.1mol,铁与足量水蒸气反应生成四氧化三铁,铁的化合价升高到+
=0.1mol,铁与足量水蒸气反应生成四氧化三铁,铁的化合价升高到+![]() ,0.1molFe转移电子物质的量为0.1mol×
,0.1molFe转移电子物质的量为0.1mol×![]() ,电子数为
,电子数为![]() NA,故D错误;
NA,故D错误;
故答案为A。

【题目】某化学实验小组用酸性KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件反应速率的影响,设计了如下探究实验方案:
实验 | 草酸溶液 (0.5mol/L) | 高锰酸钾 (0.5mol/L) | 稀硫酸 (0.5mol/L) | 硫酸锰 (0.5mol/L) | 温度 | 蒸馏水 |
① | 10.0 mL | 2.0 mL | 3.0 mL | 0 | 25℃ | 1.0 mL |
② | 10.0 mL | 2.0 mL | 3.0 mL | 1.0 mL | 25℃ | 0 |
③ | 8.0 mL | 2.0 mL | 3.0 mL | 0 | 25℃ | Vx |
④ | 10.0 mL | 2.0 mL | 3.0 mL | 0 | 35℃ | 1.0 mL |
回答下列问题:
(1)本方案中用于设计实验的化学反应的离子方程式是____,实验中预计通过观察什么现象或测定什么数据来进行判断:_____。
(2)该实验的目的是____。
(3)实验③中的Vx=____;实验①和④测得反应速率分别为v1、v4,则v1____v4(填:“>”“<”和“=”)
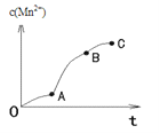
(4)实验①中,c(Mn2+)与t关系如图所示。AB段斜率明显大于OA段斜率,除反应可能放热外,猜想还可能是_____,利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1 mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
①补全实验III的操作:向试管中先加入1mL 0.01mol/L酸性KMnO4溶液,再加入10滴3mol/L硫酸,然后加入少量的____,最后加入1mL 0.1 mol/L草酸溶液。
②若猜想成立,应观察到的实验现象是_______。