题目内容
【题目】下列实验方案不能达到相应目的的是( )
目的 | A.验证牺牲阳极的阴极保护法 | B.研究浓度对FeCl3水解平衡的影响 |
实验方案 |
|
|
目的 | C.比较CH3COOH和H3BO3(硼酸)酸性的强弱 | D.比较AgCl和AgI溶解度的大小 |
实验方案 |
|
|
A.AB.BC.CD.D
【答案】D
【解析】
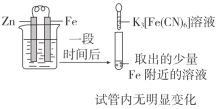
A.Zn和Fe相连插入电解质溶液中,形成原电池。一段时候,取Fe附近的溶液,加入K3[Fe(CN)6]检验Fe2+,试管内无明显变化,说明Fe没有被腐蚀,Zn保护了Fe防止Fe被腐蚀,验证了牺牲阳极的阴极保护法,能达到实验目的,A不符合题意;
B.如果水解平衡不移动,0.1mol·L-1FeCl3溶液稀释10倍后,pH会从1.43,升高到2.43,现pH=2.19,说明稀释,促进了Fe3+的水解,能达到实验目的,B不符合题意;
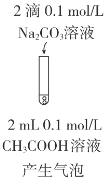
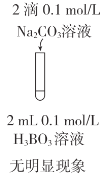
C.向相同浓度的CH3COOH溶液和H3BO3溶液中,滴加相同量的Na2CO3溶液,醋酸溶液中有气泡,生成了CO2,说明醋酸酸性强于碳酸;而硼酸溶液中没有明显现象,说明硼酸酸性弱于碳酸;该实验能达到实验目的,C不符合题意;
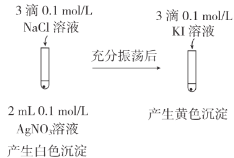
D.利用沉淀的转化来验证AgCl和AgI溶解度大小,一般情况下,难溶的电解质能够转化为更难溶的电解质。向2mL0.1mol·L-1AgNO3溶液中滴加3滴0.1mol·L-1NaCl溶液,溶液中Ag+过量,再滴加KI溶液,Ag+会与I-直接反应生成AgI沉淀,而不是AgCl沉淀转化为AgI沉淀,不能验证AgCl和AgI溶解度大小,D符合题意;
答案选D。

【题目】羰基硫(COS)可用作粮食熏蒸剂,可由CO和H2S在一定条件下反应制得。在2L的密闭容器中发生反应CO(g)+H2S(g)![]() COS(g)+H2(g),有关数据如表所示:
COS(g)+H2(g),有关数据如表所示:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(CO) | n(H2S) | n(CO) | ||
① | 150 | 10 | 10 | 7 |
② | 400 | 20 | 20 | 16 |
下列说法正确的是( )
A.②中CO的平衡转化率为80%
B.400℃时该反应的平衡常数K=![]()
C.该反应是吸热反应
D.①中反应10min达到平衡,0~10min的平均反应速率:v(CO)=0.3mol/(Lmin)