题目内容
【题目】甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)=CH3OH(g) △H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)=CO(g)+H2O(g) △H3
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
![]()
由此计算△H1=kJ.mol-1,
已知:△H2=-58kJ.mol-1,则△H3=kJ.mol-1
(2)反应①的化学平衡常数K的表达式为_____________;图1中能正确反映平衡常数K随温度变化关系的曲线为____________(填曲线标记字母),其判断理由是____________。
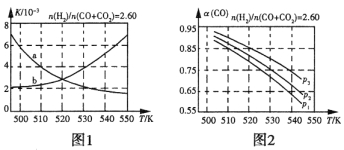
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而_____________(填“增大”或“减小”),其原因是_____________。图2中的压强由大到小为___________,其判断理由是____________。
【答案】
(1)—99;+41
(2)![]() ;a;反应①为放热反应,平衡常数应随温度升高变小;
;a;反应①为放热反应,平衡常数应随温度升高变小;
(3)减小;升高温度时,反应①为放热反应,平衡向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又产生CO的量增大;总结果,随温度升高,使CO的转化率降低;P3>P2>P1;相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响,故增大压强时,有利于CO的转化率升高。
【解析】
试题分析:(1)反应热=反应物总键能-生成物总键能,故△H1=1076 kJ.mol-1 + 2 × 436 kJ.mol-1-(3 × 413 + 343 + 465) kJ.mol-1 = -99 kJ.mol-1;根据盖斯定律:反应②-反应①=反应③,故△H3=△H2-△H1=-58kJ.mol-1-(-99kJ.mol-1)=+41kJ.mol-1,故答案为:-99;+41;
(2)反应①CO(g)+2H2(g)![]() CH3OH(g)的平衡常数表达式K=
CH3OH(g)的平衡常数表达式K=![]() ;反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,曲线a正确反映平衡常数K随温度变化关系,故答案为:
;反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,曲线a正确反映平衡常数K随温度变化关系,故答案为:![]() ;a;反应①正反应为放热反应,平衡常数随温度升高而减小;
;a;反应①正反应为放热反应,平衡常数随温度升高而减小;
(3)由图可知,压强一定时,随温度的升高,CO的转化率减小,反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡体系中CO的量增大,反应③为吸热反应,升高温度,平衡向正反应方向移动,又使平衡体系中CO的增大,总结果,随温度升高,CO的转化率减小;相同温度下,反应③前后气体分子数不变,压强改变不影响其平衡移动,反应①正反应为气体分子数减小的反应,增大压强,有利于平衡向正反应方向移动,CO的转化率增大,故增大压强有利于CO的转化率升高,故压强:P1>P2>P3,故答案为:减小;反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡体系中CO的量增大,反应③为吸热反应,升高温度,平衡向正反应方向移动,又使平衡体系中CO的增大,总结果,随温度升高,CO的转化率减小;P1>P2>P3;相同温度下,反应③前后气体分子数不变,压强改变不影响其平衡移动,反应①正反应为气体分子数减小的反应,增大压强,有利于平衡向正反应方向移动,CO的转化率增大,故增大压强有利于CO的转化率升高。

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案