题目内容
【题目】下列有关实验的选项正确的是( )
|
|
|
|
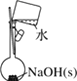
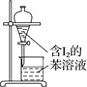
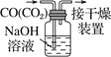
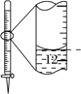
A.配制0.10mol·L-1NaOH溶液 | B.苯萃取碘水中I2,分出水层后的操作 | C.除去CO中的CO2 | D.记录滴定终点读数为12.20mL |
A.AB.BC.CD.D
【答案】C
【解析】
A.容量瓶是准确配制一定物质的量浓度溶液的仪器,要在烧杯中溶解固体物质,不能在容量瓶中进行固体的溶解,A错误;
B.进行萃取分液,下层液体从下口流出,上层液体要从上口倒出,由于苯层在上层,所以应在分出水层后从分液漏斗的上口倒出该溶液,B错误;
C.CO2是酸性氧化物,可以与NaOH反应产生可溶性盐和水,而CO不能反应,所以可利用NaOH吸收CO中的二氧化碳,可以达到除杂净化的实验目的,C正确;
D.滴定管0刻度在上部,小刻度在上,大刻度在下,液面读数是在11.80mL刻度处,D错误;
故选C。

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案【题目】根据下列操作、现象,所得结论正确的是![]()
选项 | 操作 | 现象 | 结论 |
A | 向25mL冷水和沸水中分别滴入5滴 | 前者为黄色. 后者为红褐色 | 温度升高, 程度增大 |
B | NaOH的乙醇溶液与溴乙烷共热,产生的气体通入 酸性高锰酸钾溶液中 | 溶液褪色 | 产生的气体为乙烯 |
C | 铜铝合金加入一定量稀硝酸中,有金属剩余,再加稀硫酸 | 剩余金属质量减小 | 铝与稀硫酸反应使 剩余金属质量减小 |
D | 盛有 | 气体变为无色 |
|
A.AB.BC.CD.D
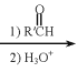
【题目】在一定温度下,10 mL 0.50 mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
v(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.1 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:v(H2O2)≈0.033 mol/(L·min)
B.6~10 min的平均反应速率:v(H2O2)>3.3×10-2 mol/(L·min)
C.反应到6 min时,H2O2分解了40%
D.反应到10 min时,c(H2O2)≈0.24 mol/L