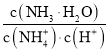题目内容
【题目】工业上可采用CO和H2合成甲醇,发生的反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0,若该反应在绝热、恒容的密闭容器中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是( )
CH3OH(g) ΔH<0,若该反应在绝热、恒容的密闭容器中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是( )
A.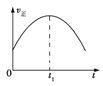
B.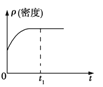
C.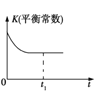
D.
【答案】C
【解析】
A.随着反应的进行,反应物浓度减小、温度升高,正反应速率改变,当正反应速率不变时该反应达到平衡状态,t1时刻该反应没有达到平衡状态,故A错误;
B.混合气体的质量和体积均始终不变,则混合气体的密度不变时,不一定为平衡状态,故B错误;
C.平衡常数只随温度变化,当平衡常数不变,说明容器内混合气体的温度不再变化,此时是平衡状态,故C正确;
D.△H只与热化学方程式有关,与反应过程无关,△H不变,无法判断是平衡状态,故D错误;
故答案为C。
化学平衡的标志有直接标志和间接标志两大类。一、直接标志:正反应速率=逆反应速率,注意反应速率的方向必须有正向和逆向。同时要注意物质之间的比例关系,必须符合方程式中的化学计量数的比值。二、间接标志:①各物质的浓度不变;②各物质的百分含量不变;③对于气体体积前后改变的反应,压强不变是平衡的标志;④对于气体体积前后不改变的反应,压强不能做标志;⑤对于恒温恒压条件下的反应,气体体积前后改变的反应密度不变是平衡标志;⑥对于恒温恒容下的反应,有非气体物质的反应,密度不变是平衡标志。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
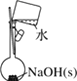
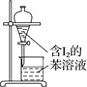
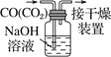
【题目】下列有关实验的选项正确的是( )
|
|
|
|
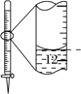
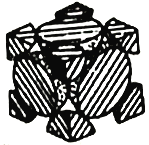
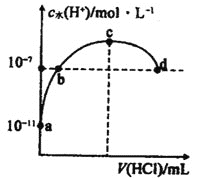
A.配制0.10mol·L-1NaOH溶液 | B.苯萃取碘水中I2,分出水层后的操作 | C.除去CO中的CO2 | D.记录滴定终点读数为12.20mL |
A.AB.BC.CD.D