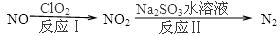题目内容
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
(1)已知:ⅰ.反应A中,4 molHCl被氧化,放出115.6 kJ的热量。
ⅱ.

①H2O的电子式是________。
②反应A的热化学方程式是______________________________________。
③断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”)________。
(2)对于反应A,下图是在4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。

①曲线b对应的投料比是________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投料比的关系是______________________________。
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是________。
反应A:4HCl+O2
 2Cl2+2H2O
2Cl2+2H2O(1)已知:ⅰ.反应A中,4 molHCl被氧化,放出115.6 kJ的热量。
ⅱ.

①H2O的电子式是________。
②反应A的热化学方程式是______________________________________。
③断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”)________。
(2)对于反应A,下图是在4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。

①曲线b对应的投料比是________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投料比的关系是______________________________。
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是________。
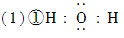
②4HCl(g)+O2(g)
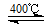 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)ΔH=-115.6 kJ/ mol
③32 强
(2)①4:1
②投料比越高,对应的反应温度越低
③30.8%
(1)③设H—O键的键能为x,H—Cl键的键能为y,则有-115.6=-2×243-4x+4y+498,化简得x-y=31.9,即断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为32 kJ,H2O中H—O键比HCl中H—Cl键强。
(2)①同一温度下,O2的浓度越大,HCl的平衡转化率越高,故曲线a、d分别对应n(HCl):n(O2)为6:1、1:1的情况,曲线b对应的投料比是4:1。
②在图上作一平行于温度轴的直线与曲线b、c、d相交,可以看出,当不同投料比下HCl的平衡转化率相同时,曲线b对应的温度最低,曲线d对应的温度最高。则可得出结论:投料比越高,对应的反应温度越低。
③此时HCl的平衡转化率为80%。设反应开始时n(HCl)=2a mol,n(O2)=a mol。
4HCl(g)+O2(g)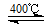 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)
起始 2a mol a mol 0 0
转化 1.6a mol 0.4a mol 0.8a mol 0.8a mol
平衡 0.4a mol 0.6a mol 0.8a mol 0.8a mol
则平衡混合气体中Cl2的物质的量分数是
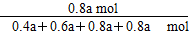 ×100%≈30.8%。
×100%≈30.8%。
(2)①同一温度下,O2的浓度越大,HCl的平衡转化率越高,故曲线a、d分别对应n(HCl):n(O2)为6:1、1:1的情况,曲线b对应的投料比是4:1。
②在图上作一平行于温度轴的直线与曲线b、c、d相交,可以看出,当不同投料比下HCl的平衡转化率相同时,曲线b对应的温度最低,曲线d对应的温度最高。则可得出结论:投料比越高,对应的反应温度越低。
③此时HCl的平衡转化率为80%。设反应开始时n(HCl)=2a mol,n(O2)=a mol。
4HCl(g)+O2(g)
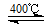 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)起始 2a mol a mol 0 0
转化 1.6a mol 0.4a mol 0.8a mol 0.8a mol
平衡 0.4a mol 0.6a mol 0.8a mol 0.8a mol
则平衡混合气体中Cl2的物质的量分数是
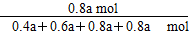 ×100%≈30.8%。
×100%≈30.8%。
练习册系列答案
相关题目
 O2(g)=CO(g)ΔH=-393.5 kJ·mol-1
O2(g)=CO(g)ΔH=-393.5 kJ·mol-1 Si(s)+4HCl(g)ΔH=+Q kJ·mol-1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )。
Si(s)+4HCl(g)ΔH=+Q kJ·mol-1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )。

 2CO2(g)+N2(g),已知该反应在570K时的平衡常数为1×1059,但反应速率极慢。下列说法正确的是:________
2CO2(g)+N2(g),已知该反应在570K时的平衡常数为1×1059,但反应速率极慢。下列说法正确的是:________
 Ni(CO)4(g),镍与CO反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2除去CO,生成物为S和CO2。已知相关反应过程的能量变化如图所示
Ni(CO)4(g),镍与CO反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2除去CO,生成物为S和CO2。已知相关反应过程的能量变化如图所示

 2N2(g)+3H2O(g)△H<0。为提高氮氧化物的转化率可采取的措施是(任意填一种)____________________。
2N2(g)+3H2O(g)△H<0。为提高氮氧化物的转化率可采取的措施是(任意填一种)____________________。