题目内容
13.完成下列化学用语:①NaHCO3在溶液中的电离方程式NaHCO3=Na++HCO3-
②以石墨为电极电解某铜盐溶液的离子方程式为2Cu2++2H2O$\frac{\underline{\;通直流电\;}}{\;}$ 2Cu+O2↑+4H+,则相应的化学方程式可以是(写一例)2Cu(NO3)2+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4HNO3
③若实验室没有给酒精灯等热源,某同学在试管中将液溴、苯及铁屑相混合,若有化学反应发生,写出化学方程式,若无反应发生,则说明理由苯与液溴发生取代反应,铁屑作催化剂,该反应为放热反应,发生C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr
④以Pb作电极电解醋酸的浓溶液,在电解过程中,无沉淀产生,但电解效率逐渐下降,同时H+浓度也随之降低,随后溶液不再导电,电解自然停止,阳极电极反应式是4OH--4e-=2H2O+O2↑.
分析 ①碳酸氢钠为强电解质,在水中电离产生钠离子和碳酸氢根离子;
②根据以石墨为电极电解某铜盐溶液的离子方程式可知电解的本质为电解铜离子和水,据此书写相应的化学方程式;
③苯与液溴发生取代反应,铁屑作催化剂,该反应为放热反应,液溴、苯及铁屑相混合,生成溴苯和HBr;
④乙酸为弱酸,根据离子的放电顺序:电解乙酸溶液阳极氢氧根离子放电,阴极氢离子放电,据此分析解答.
解答 解:①碳酸氢钠为强电解质,在水中电离产生钠离子和碳酸氢根离子,电离方程式为:NaHCO3=Na++HCO3-,
故答案为:NaHCO3=Na++HCO3-;
②以石墨为电极电解某铜盐溶液:2Cu2++2H2O$\frac{\underline{\;通直流电\;}}{\;}$ 2Cu+O2↑+4H+,电解的本质为电解铜离子和水,阳极:4OH--4e-=O2↑+2H2O,阴极:2Cu2++4e-=2Cu,根据溶液中离子的放电顺序:OH->NO3-,所以该铜盐可以是硝酸铜,反应为:2Cu(NO3)2+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4HNO3,
故答案为:2Cu(NO3)2+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4HNO3;
③在试管中将液溴、苯及铁屑相混合,首先是液溴与铁反应生成溴化铁放热,溴化铁和苯反应生成溴苯和铁放热,所以实验室没有给酒精灯等热源,将液溴、苯及铁屑相混合,苯与液溴发生取代反应生成溴苯和HBr,反应为C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr,
故答案为:苯与液溴发生取代反应,铁屑作催化剂,该反应为放热反应,发生C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
④根据离子的放电顺序可知,在电解醋酸溶液时,阴极上H+放电,电极反应式为:2H++2e-=H2↑;阳极上氢氧根离子放电,电极反应式为:4OH--4e-═H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑.
点评 本题考查电离方程式的书写、电解原理的应用,为高频考点,把握物质的性质及发生的化学反应为解答的关键,注意电解时溶液中离子的放电顺序,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 摩尔是七个基本物理量之一,其单位 mol | |
| B. | 1mol任何物质都含有6.02×1023个分子 | |
| C. | 气体的摩尔体积为22.4L | |
| D. | 摩尔质量在数值上等于该物质的相对分子质量或相对原子质量 |
| A. | 某固体中加入稀盐酸,产生了无色无味且能使澄清石灰水变浑浊的气体,证明该固体中一定含有CO32- | |
| B. | 验证溶液中是否含有Cl-,加稀硝酸酸化的AgNO3溶液,有白色沉淀,证明含Cl- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 加入Ba(NO3)2溶液生成白色沉淀,再加稀盐酸酸化沉淀不消失,证明一定含有SO42- |
| A. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑ | |
| B. | 3S+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$2K2S+K2SO3+3H2O | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+H2O | |
| D. | O3+2KI+H2O=2KOH+I2+O2 |
| A. | 配制硫酸溶液时,可在量筒中加入一定体积的浓硫酸,再在搅拌条件下慢慢加入水 | |
| B. | 蒸馏时,冷凝管内的冷却水从下口进、上口出 | |
| C. | 不慎将酸溅到眼睛中,应立即用大量水冲洗,边洗边眨眼睛 | |
| D. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
①沸点比较:丙烷>乙烷>甲烷
②
 互为同分异构体.
互为同分异构体.③钠与乙醇的反应,液溴与苯的反应均可属于取代反应.
④丁烷与异丁烷互为同系物.
⑤甲烷和苯不能使酸性KMnO4溶液褪色,裂化汽油能使酸性KMnO4溶液褪色.
| A. | 全部 | B. | ①②③⑤ | C. | ①③⑤ | D. | ②③④ |
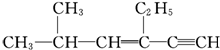 ,有关其分子结构的叙述中正确的是( )
,有关其分子结构的叙述中正确的是( )| A. | 分子中一定在同一平面上的碳原子数为6 | |
| B. | 分子中一定在同一平面上的碳原子数为7 | |
| C. | 分子中在同一直线上的碳原子数为6 | |
| D. | 分子中在同一直线上的碳原子数为4 |
