题目内容
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是
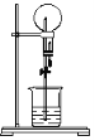
A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
D.HCl、NH3和SO2均能用该装置做喷泉实验
【答案】C
【解析】
A. 利用氨气极易溶于水,造成烧瓶内压强减小,从而形成喷泉,故A说法正确;
B. 选用NaOH等溶液,利用CO2与NaOH溶液发生反应,造成烧瓶内压强减小,能形成喷泉,故B说法正确;
C. NO2与水反应:3NO2+H2O=2HNO3+NO,NO不与水反应,即稀硝酸不能充满烧瓶,故C说法错误;
D. HCl、NH3极易溶于水,可以用改装置做喷泉实验,将溶液换成氢氧化钠溶液,SO2也能用该装置做喷泉实验,故D说法正确;
答案:C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目