题目内容
【题目】在标准状况下,将aLHCl(气)溶于1L水中(水的密度为1gcm﹣3),得到的盐酸的密度为bgmL﹣1,质量分数为w,物质的量浓度为cmolL﹣1则下列关系式中不正确的是
A.w=![]()
B.w=![]()
C.C=![]()
D.b=![]()
【答案】D
【解析】
试题分析:A.w=(溶质的质量)÷(溶液的质量)×100%=![]() ,故A正确;B.假设溶液为1L,根据w=(溶质的质量)÷(溶液的质量)×100%=
,故A正确;B.假设溶液为1L,根据w=(溶质的质量)÷(溶液的质量)×100%=![]() ,故B正确;C.标准状况下的aLHCl(气)的物质的量为
,故B正确;C.标准状况下的aLHCl(气)的物质的量为![]() =
=![]() mol,氯化氢的质量为
mol,氯化氢的质量为![]() mol×36.5g/mol=
mol×36.5g/mol=![]() g;所以溶液质量为1000g+
g;所以溶液质量为1000g+![]() g=(1000+
g=(1000+![]() )g,所以溶液的体积为
)g,所以溶液的体积为![]() =
=![]() mL,所以溶液浓度为
mL,所以溶液浓度为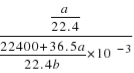 =
=![]() mol/L,故C正确;
mol/L,故C正确;
D.气体溶于水后体积不是a+1L,故D错误,故选D。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
【题目】
(1)需要称量NaOH固体 克;
(2)需量取密度为1.19g/cm3、质量分数为36.5%的浓盐酸________mL;
(3)定容时的操作是:继续向容量瓶中加蒸馏水至 ,改用胶头滴管滴加蒸馏水至 。
(4)配制过程中,下列实验操作导致所配制的稀盐酸的物质的量浓度偏大的有 。
A.量取浓盐酸时发现量筒不干净,用水洗净后直接量取 |
B.用量筒量取浓盐酸时仰视观察凹液面 |
C.稀释浓盐酸时,没有冷却就立即转移到容量瓶中 |
D.定容时俯视刻度线 |
E.加蒸馏水时不慎超过了刻度线,用胶体滴管吸出
F.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水