��Ŀ����
����Ŀ��ʵ������Ҫ0.1 mol��L��1 NaOH��Һ450 mL��0.5 mol��L��1������Һ500 mL��������������Һ����������ش��������⣺
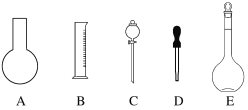
��1������ͼ��ʾ��������������Һ�϶�����Ҫ����____________________(����ĸ)��
������������Һ�����õ��IJ���������__________________(����������)��
�������й�����ƿʹ��˵������ȷ������ ��
a������ƿʹ��ǰһ��Ҫ����Ƿ�©Һ�������Ϊװˮ����ƿ���������۲��Ƿ�©ҹ����������������ת180����������۲��Ƿ�©ҹ��
b��������Ϊ��Ӧ��������������Һ�����������ǿ������������������Һ��
c�����ܽ������Ũ��Һֱ��������ƿ���ܽ��ϡ�ͣ����ܼ���������ȵ�Һ�� ��
d��������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫС��
(2)������NaOH��Һʱ��
�ٸ��ݼ�����������ƽ��ȡNaOH������Ϊ________g��
����NaOH��Һ��ת��������ƿʱ����������������������ҺŨ��___________(�>������<������)0.1 mol��L��1��
����NaOH�����ܽ��������������ƿ��ϴ���ձ�����������ϴ��Һ��������ƿ�����ݣ���������ҺŨ��___________(�>������<������) 0.1 mol��L��1��
(3)������������Һʱ��
��������������Ϊ98%���ܶ�Ϊ1.84 g��cm��3��Ũ��������Ϊ__________(����������һλС��)mL��
�����ʵ������15 mL��50 mL��100 mL��Ͳ��Ӧѡ��___________mL��Ͳ��ã�
�����ƹ������������ձ��н�Ũ�������ϡ�ͣ�ϡ��ʱ����������__________________________��
���𰸡�(1)AC �ձ��������� bd
(2)��2.0��2�֣� ��<��2�֣� ��>��2�֣�
(3)��13.6��2�֣� ��15��2�֣� �۽�Ũ���������ڻ�������ˮ�У����ò��������Ͻ�����2�֣�
��������
�����������1����������Һ��Ҫ���ֲ�����������Ͳ���ձ�������������ͷ�ιܡ�����ƿ������Ҫ������ƿ�ͷ�Һ©����
���������Ϸ�����֪����Ҫ���������ձ��Ͳ�������
��a������ƿʹ��ǰһ��Ҫ����Ƿ�©Һ�������Ϊװˮ����ƿ���������۲��Ƿ�©ҹ����������������ת180����������۲��Ƿ�©ҹ��a��ȷ��b��������Ϊ��Ӧ��������������Һ��������ֻ������һ���������Һ��b����c�����ܽ������Ũ��Һֱ��������ƿ���ܽ��ϡ�ͣ����ܼ���������ȵ�Һ����c��ȷ��d��������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫ��d����ѡbd��
��2��������450 mL������ƿ������NaOH��ҺҪ��500 mL������ƿ��m��NaOH��=cVM=0.1 molL-1��0.5 L��40 gmol-1=2.0 g��
����NaOH��Һ��ת��������ƿʱ����������������������ҺŨ��ƫС����С��0.1mol/L��
��NaOH����ˮ�ų������ȣ�Ӧ������ȴ�����º�����������ƿ�У������ݺ���Һ��ȴ�����º������С��Ũ��ƫ�ߣ�
��3����c��Ũ��V��Ũ��=c��ϡ��V��ϡ������1000��1.84��98%/98��V��Ũ��=0.5��0.5������V��Ũ����0.013 6 L=13.6 mL����ѡ��15 mL��Ͳ��ã����С����Ũ��������ˮ���ȣ����ܶȴ���ˮ������ϡ��Ũ����IJ���Ϊ����Ũ���������ڻ�������ˮ�У����ò��������Ͻ�����

 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�