题目内容
【题目】已知:工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g) △H<0。下列事实不能用勒夏特列原理解释的是( )
2NH3(g) △H<0。下列事实不能用勒夏特列原理解释的是( )
A.温度过高对合成氨不利
B.合成氨在高压下进行是有利的
C.高温及加入催化剂都能使合成氨的反应速率加快
D.增加N2的浓度可提高平衡混合物中NH3的产量
【答案】C
【解析】
试题分析:A.该反应的正逆反应是放热反应,温度越高,平衡逆向移动,对合成氨不利,所以可以用平衡移动原理解释,错误;B.该反应前后气体的物质的量之和减小,增大压强,平衡正向移动,所以合成氨在高压下进行是有利的,可以用平衡移动原理解释,错误;C.催化剂能增大化学反应速率,但不引起平衡移动,所以不能用平衡移动原理解释,正确;D.增加氮气浓度,平衡正向移动,所以可以提高平衡混合物中氨气含量,所以可以用平衡移动原理解释,错误。

【题目】某研究小组探究SO2和Fe(NO3)3溶液的反应。请回答:
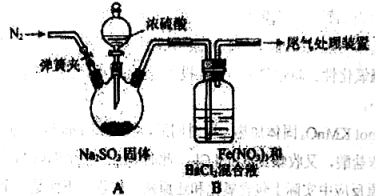
(1)A中滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N2,再关闭弹簧夹,目的是 。
(2)装置B中产生了白色沉淀,其成分是 。
已知SO2不与BaCl2溶液反应,该研究小组对产生白色沉淀的原因进行了假设:
假设1:SO2与Fe3+反应;
假设2:在酸性条件下SO2与NO3-反应;
假设3: 。
【设计方案、验证假设】
(3)某同学设计实验验证假设2,请帮他完成下表中内容。
实验步骤 | 预期的现象和结论 |
①测定B中实验所用混合溶液的__________ ②配制具有相同 的稀硝酸与BaCl2的混合液并通入适当的 ③将SO2通入上述溶液中 | 若出现白色沉淀则假设2成立 若不出现白色沉淀则假设2不成立 |
经验证假设2成立,则验证过程中发生的离子方程式是 。
(提示:NO3-在不同条件下的还原产物较复杂,此条件未见气体产生)
【思考与交流】
若假设1、假设2都成立,你是否同意假设3,并简述理由 。
【题目】下列有关物质的性质与用途具有对应关系的是
性质 | 用途 | |
A | 液氨气化吸热 | 可用作制冷剂 |
B | NH4HCO3受热易分解 | 可用作氮肥 |
C | 二氧化硅能与HF反应 | 可用作光导纤维 |
D | 二氧化硫能使溴水褪色 | 可用作漂白剂 |
A. A B. B C. C D. D