题目内容
9.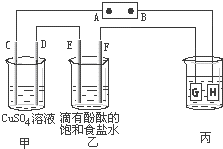 如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:
(1)A极是电源的正,甲装置观察到的现象是C极表面有气泡逸出、
D极有红色物质析出、电解质溶液蓝色变浅.
(2)C极的电极反应式为4OH--4e-=2H2O+O2↑.
(3)现用丙装置给铜件镀银,则H应该是镀件(填“镀层金属”或“镀件”),电镀液是AgNO3溶液.
分析 C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极,将直流电源接通后,F极附近呈红色,说明F电极附近有碱生成,则F电极上氢离子放电生成氢气,为阴极,所以C、E、G是阳极,D、F、H是阴极,连接阳极的电极A是正极、连接阴极的电极B是负极;
(1)甲中阳极上氢氧根离子放电生成无色气体,阴极上铜离子放电生成Cu单质,随着反应的进行,溶液中铜离子浓度降低;
(2)C是阳极,C电极上氢氧根离子放电生成氧气;
(3)丙装置是电镀池,镀层Ag为阳极、镀件Cu为阴极,电镀液是硝酸银溶液.
解答 解:(1)C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极,将直流电源接通后,F极附近呈红色,说明F电极附近有碱生成,则F电极上氢离子放电生成氢气,为阴极,所以C、E、G是阳极,D、F、H是阴极,连接阳极的电极A是正极、连接阴极的电极B是负极;
甲中阳极上氢氧根离子放电生成无色气体,阴极上铜离子放电生成Cu单质,随着反应的进行,溶液中铜离子浓度降低,所以看到的现象是:C极表面有气泡逸出、D极有红色物质析出、电解质溶液蓝色变浅,
故答案为:正;C极表面有气泡逸出;D极有红色物质析出;电解质溶液蓝色变浅;
(2)C是阳极,C电极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑;
(3)丙装置是电镀池,镀层Ag为阳极、镀件Cu为阴极,电镀液是硝酸银溶液,G是阳极、H是阴极,所以G是镀层Ag、H是镀件Cu,电镀液是硝酸银溶液,
故答案为:镀件;AgNO3.
点评 本题考查电解原理,正确判断阴阳极及正负极是解本题关键,知道各个电极上发生的反应,会正确书写电极反应式,题目难度不大.

| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
| A. | 能跟硝酸发生化合反应 | |
| B. | 能跟硝酸发生酯化反应 | |
| C. | 能跟乙酸反应生成乙酸酯 | |
| D. | 1mol单糖单元必定和3mol硝酸发生反应,少于3mol则不能反应 |
①Na与水反应时,增大水的用量
②做铝与氧气反应的实验时,将铝片改为铝粉
③Zn与稀H2SO4反应式,滴加少量CuSO4溶液
④常温下Fe与稀硫酸反应制取氢气时,改用浓硫酸
⑤用H2O2制取O2时,加入少量MnO2.
| A. | ①②④ | B. | ②③④ | C. | ①④⑤ | D. | ②③⑤ |
| A. | 氢氟酸保存在玻璃试剂瓶中 | B. | 氯水保存在棕色试剂瓶中 | ||
| C. | 金属钠保存在无水酒精中 | D. | 浓硝酸保存在无色试剂瓶中 |
| A. | 香烟烟气中只有尼古丁有毒 | |
| B. | 市售香烟通常装有过滤嘴,所以吸烟对人体无害 | |
| C. | 吸烟只影响自己的健康,不影响他人的健康 | |
| D. | 香烟烟气中的一氧化碳比氧气更容易与血红蛋白结合 |
| A. | 浓H2SO4(热) | B. | 浓HNO3(常温) | C. | 浓盐酸(热) | D. | 稀HNO3(热) |
| A. | 通入足量溴水中 | B. | 点燃 | ||
| C. | 催化加氢 | D. | 通入足量酸性KMnO4溶液中 |
| A. | 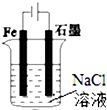 图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红 | |
| B. | 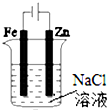 图②装置可以验证牺牲阳极的阴极保护法 | |
| C. |  图③可以模拟钢铁的吸氧腐蚀,铁棒一极的电极反应式:Fe=Fe 2++2e- | |
| D. | 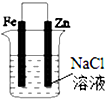 分别给上述4个装置的铁电极附近滴加少量K3[Fe(CN)6]溶液,②④出现蓝色沉淀 |